Trái Đất vào khoảng 500 triệu năm tuổi dường như chẳng có gì là đặc biệt so với các hành tinh khác trong hệ Mặt Trời. Trái Đất sở hữu những rặng núi lửa khổng lồ chỉ chực chờ phun trào, nhưng các hành tinh khác cũng vậy. Trái Đất thì được bao phủ bởi những đại dương rộng lớn trải dài cho đến tận chân trời, nhưng sao Hỏa trong khoảng thời gian này cũng đã có những vùng biển chẳng thua kém gì so với Trái Đất (trước khi bị bốc hơi hoàn toàn). Thậm chí, các vệ tinh khổng lồ của sao Mộc như Europa và Callisto còn được bao bọc bởi những đại dương sâu hơn 80km bị che lấp bởi một lớp băng dày.
Bạn cũng có thể lập luận rằng các hoạt động kiến tạo mảng – một quá trình giúp biến đổi triệt để bề mặt hành tinh của chúng ta – là một điểm khác biệt rõ rệt, nhưng trong những năm tháng này, sao Kim và sao Hỏa cũng đã có riêng cho mình những hoạt động địa chất tương tự.
Hóa học cũng chẳng phải là yếu tố tạo nên sự khác biệt cho Trái Đất. Đá bazan và đá granit chiếm ưu thế tuyệt đối ở các hành tinh đất đá – cùng với “bộ sáu kỳ diệu” bao gồm oxy, silic, nhôm, magie, canxi và sắt. Trái Đất cũng đã có cacbon, nitơ và lưu huỳnh, nhưng các hành tinh khác trong Hệ Mặt Trời cũng chẳng “đói khát” gì các nguyên tố này.
Như vậy, dựa vào khá nhiều tiêu chí, chúng ta có thể thấy rằng Trái Đất cách đây bốn tỷ năm dường như là một hành tinh rất đỗi bình thường. Nhưng Trái Đất lại “sắp” mang trong mình một yếu tố rất đặc biệt – một yếu tố đã làm cho hành tinh này trở nên độc nhất vô nhị cho đến tận ngày nay. Vậy thì yếu tố đó là gì?
1. Sự sống là gì?
Mình đang sống, bạn cũng đang sống, mọi người xung quanh bạn cũng đang sống (và làm việc). Rộng hơn nữa thì tất cả các loài sinh vật – từ vật nuôi như con chó hay con mèo trong nhà của bạn – cho tới các loài sinh vật hoang dã trên hành tinh này như hổ, beo, vượn, cáo, chim chóc…, tất cả đều đang sống, đang hít thở, đang ăn uống hay ngủ nghỉ…Nhưng chính xác thì sự sống là gì?
Câu hỏi này nghe có vẻ thật là ngớ ngẩn và nực cười (thì chúng ta đang sống nhăn răng ra đây thì cần gì phải hỏi!) nhưng rất khó để có thể đưa ra được một câu trả lời hoàn toàn chính xác. Sau đây là một ví dụ nhỏ: mặc dù virus có thể tấn công các sinh vật sống, gây bệnh hay thậm chí là sinh sản, nhưng chúng lại không được cấu tạo từ các tế bào nhỏ hơn, không thể tự mình duy trì một trạng thái ổn định ở “bên trong” hay không thể tự mình sinh trưởng và tạo ra năng lượng một cách “tự túc”.
Như vậy, chúng ta cần phải có cho mình một bộ “tiêu chí” để có thể định nghĩa về sự sống. Và sau đây là 8 đặc điểm chính giúp làm nên một sinh vật sống.
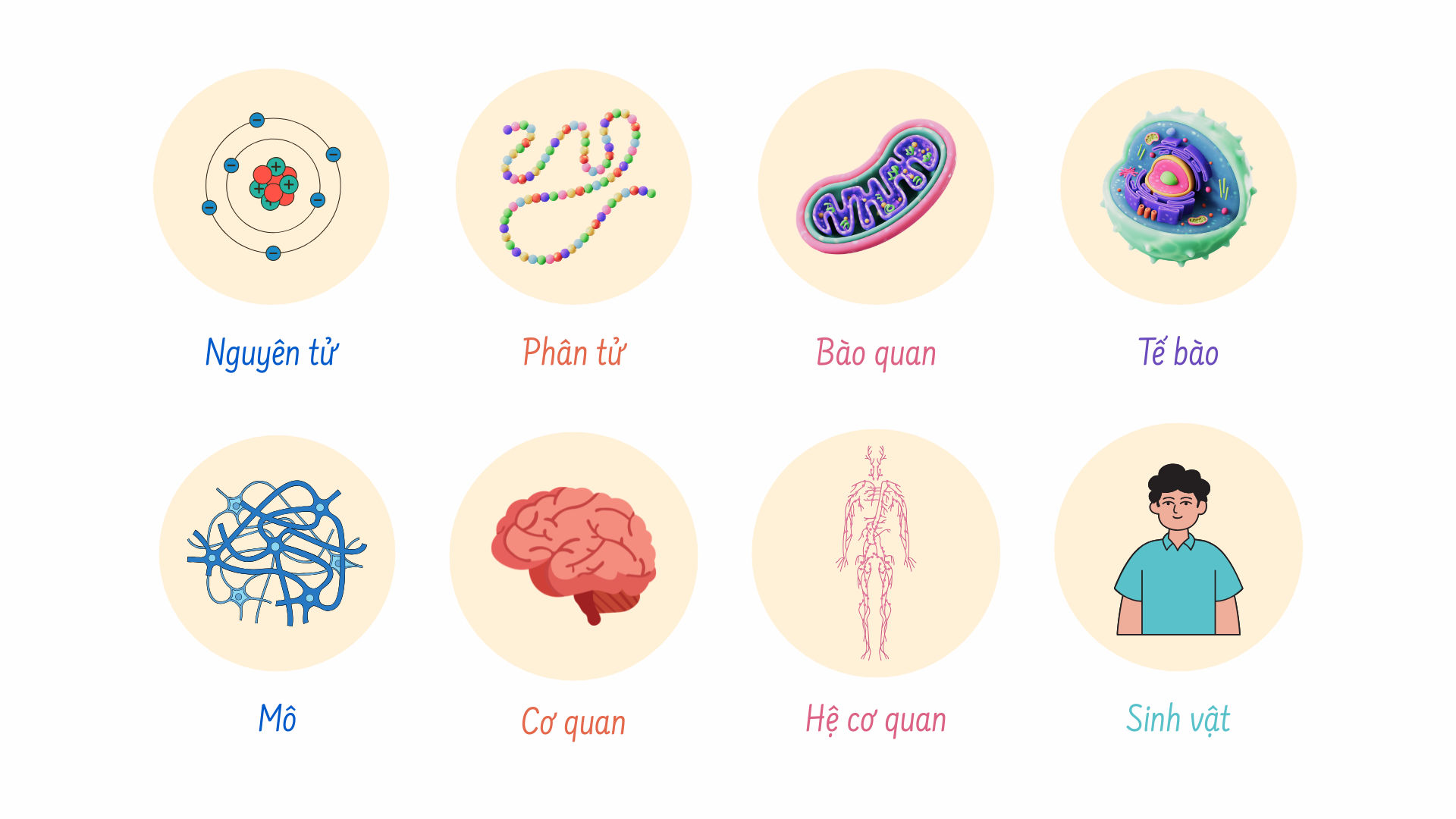
Đầu tiên, sinh vật (có sự sống) là những cấu trúc sinh học được tổ chức và phối hợp rất chặt chẽ, tuân theo một hệ thống mà chúng ta có thể phân tích trên quy mô từ nhỏ đến lớn. Chúng ta hãy bắt đầu với nguyên tử – bao gồm một hạt nhân được bao quanh bởi các electron. Các nguyên tử này sau đó sẽ tạo thành các phân tử – một cấu trúc bao gồm ít nhất hai nguyên tử liên kết với nhau bằng các liên kết hóa học, từ đó giúp hình thành nên các bào quan, chẳng hạn như ty thể giúp cung cấp năng lượng cho các hoạt động bên trong tế bào hay lục lạp cho phép thực vật sử dụng năng lượng đến từ ánh sáng mặt trời để tạo ra đường.
Lúc này, các bào quan sẽ được hợp lại để tạo thành một tế bào – một đơn vị chức năng nhỏ nhất bên trong các sinh vật sống. Một số sinh vật chỉ có một tế bào (được gọi là sinh vật đơn bào) và số khác lại có nhiều hơn (được gọi là sinh vật đa bào).
Ở các sinh vật lớn hơn nữa, các tế bào sẽ kết hợp với nhau để tạo thành mô – một nhóm các tế bào giống nhau cùng thực hiện một chức năng nhất định. Sau đó, các mô này sẽ được nhóm lại với nhau để tạo thành các cơ quan và hệ cơ quan. Ví dụ, hệ tuần hoàn – với nhiệm vụ vận chuyển máu đi khắp cơ thể – bao gồm các cơ quan như tim và các mạch máu lớn nhỏ khác nhau. Sau đó, các hệ cơ quan này sẽ phối kết hợp với nhau để tạo thành một sinh vật, chẳng hạn như cây trong rừng hoặc người đang đọc bài viết này.
(Ngoài lề một chút) Không dừng lại ở đây, các cá thể sinh vật (trong cùng một loài) sẽ “tụ họp” tại cùng một nơi để tạo thành quần thể. Ví dụ, một khu rừng có thể có rất nhiều cây thông, được gọi chung là một quần thể thông. Và khi hàng tá các quần thể khác nhau sinh sống trong cùng một khu vực nhất định, chúng sẽ tạo nên một quần xã. Ví dụ, khu rừng thông ắt hẳn sẽ phải có thêm các quần thể hoa, côn trùng và các quần thể sinh vật khác. Lúc này, bản thân khu rừng đã trở thành một hệ sinh thái – bao gồm tất cả các sinh vật sống và các thành phần “không sống” bên trong đó, chẳng hạn như nitơ trong đất hoặc nước mưa. Ở cấp độ tổ chức cao nhất, sinh quyển là tập hợp các hệ sinh thái khác nhau, bao gồm đất, nước, thậm chí là cả khí quyển.

Thứ hai, sinh vật phản ứng với rất nhiều loại kích thích khác nhau. Ví dụ, các loài thực vật có thể nghiêng về phía nguồn sáng, leo lên hàng rào hay cụp lại khi bị chạm vào. Ngay cả các loài vi khuẩn nhỏ bé cũng có thể di chuyển tới hoặc tránh xa khỏi một số chất hóa học (hướng hoá) hoặc ánh sáng (hướng quang).

Thứ ba, sinh vật phải biết sinh sản. Các sinh vật đơn bào sinh sản bằng cách phân chia tế bào, còn các sinh vật đa bào thường tạo ra các tế bào sinh sản chuyên biệt được gọi là giao tử (tế bào trứng và tế bào tinh trùng). Sau khi thụ tinh (sự kết hợp của tế bào trứng và tế bào tinh trùng), một cá thể mới sẽ bắt đầu phát triển, mang theo những đặc điểm giống bố và mẹ của chúng.

Thứ tư, tất cả các sinh vật sống ít nhiều đều thể hiện sự “phù hợp” với môi trường sống của chúng – được gọi là khả năng thích nghi. Ví dụ, để có thể sống sót ở nhiệt độ –45°C tại Alaska (Mỹ) và Yukon (Canada), ếch gỗ đã có một chiến lược thích nghi khá độc đáo: đóng băng tới 65% lượng nước bên trong cơ thể trong vòng nhiều tháng để sống sót qua mùa đông khắc nghiệt ở phía Bắc. Khi mùa xuân đến, chúng sẽ nhanh chóng “rã đông” và tận dụng các vũng nước nhỏ ở gần đó để sinh sản trước các loài lưỡng cư khác.

Thứ năm, sau khi đã thích nghi, các sinh vật sẽ tiếp tục sinh trưởng và phát triển, từ đó đưa chúng ta tới đặc điểm…
Thứ sáu, tất cả các sinh vật ít nhiều đều cần phải có những cơ chế giúp ổn định môi trường bên trong (để có thể duy trì sự sống) và đối phó với các áp lực đến từ môi trường bên ngoài – một trạng thái được gọi là cân bằng nội môi. Ví dụ, gấu Bắc Cực và các loài động vật có vú khác sống ở vùng phương Bắc lạnh giá giữ ấm cơ thể bằng lớp lông dày và lớp mỡ đặc dưới da. Ngược lại, ở những vùng khí hậu nóng nực, các sinh vật sẽ sử dụng các chiến lược khác, chẳng hạn như đổ mồ hôi ở người hoặc lè lưỡi thở hổn hển ở chó, từ đó giúp thải bớt nhiệt dư thừa ra khỏi cơ thể.

Thứ bảy, tất cả các sinh vật đều cần phải tiếp nhận và sử dụng năng lượng cho các hoạt động trao đổi chất của chúng. Ví dụ, các loài thực vật thường thu nhận năng lượng đến từ mặt trời, chuyển hóa thành năng lượng hóa học và lưu trữ trong các mô của chúng. Sau đó, các loài động vật sẽ tiêu thụ những loại “thực phẩm” này và giải phóng năng lượng được lưu trữ ở bên trong.

Cuối cùng, sự đa dạng đến đáng kinh ngạc của sự sống trên Trái Đất là kết quả của một quá trình tiến hoá vô cùng khắc nghiệt. Và “nhiên liệu” giúp cho “guồng máy” này luôn luôn tiến về phía trước đó chính là các đột biến – những thay đổi ngẫu nhiên trong gen di truyền của các sinh vật theo thời gian. Một mặt, những đột biến này sẽ có thể giúp cho các sinh vật nhanh chóng thích nghi với môi trường sống xung quanh, từ đó gia tăng cơ hội sinh sản. Mặt khác, nếu như các đột biến này làm giảm khả năng thích nghi của sinh vật thì những cá thể này sẽ phải bị loại bỏ – một quá trình chọn lọc tự nhiên. Và cái giá phải trả sẽ chính là cái chết.
Như chúng ta đã biết, sự sống trên Trái Đất là vô cùng đa dạng và phong phú. Và nguồn cơn đem lại sự đa dạng dường như là vô tận này chính là quá trình tiến hóa. Và để có thể nhìn nhận một cách tổng quan nhất về quá trình này, cây phát sinh chủng loài – một bản tóm tắt quá trình tiến hóa của các dạng sống khác nhau trên Trái Đất, là rất cần thiết.
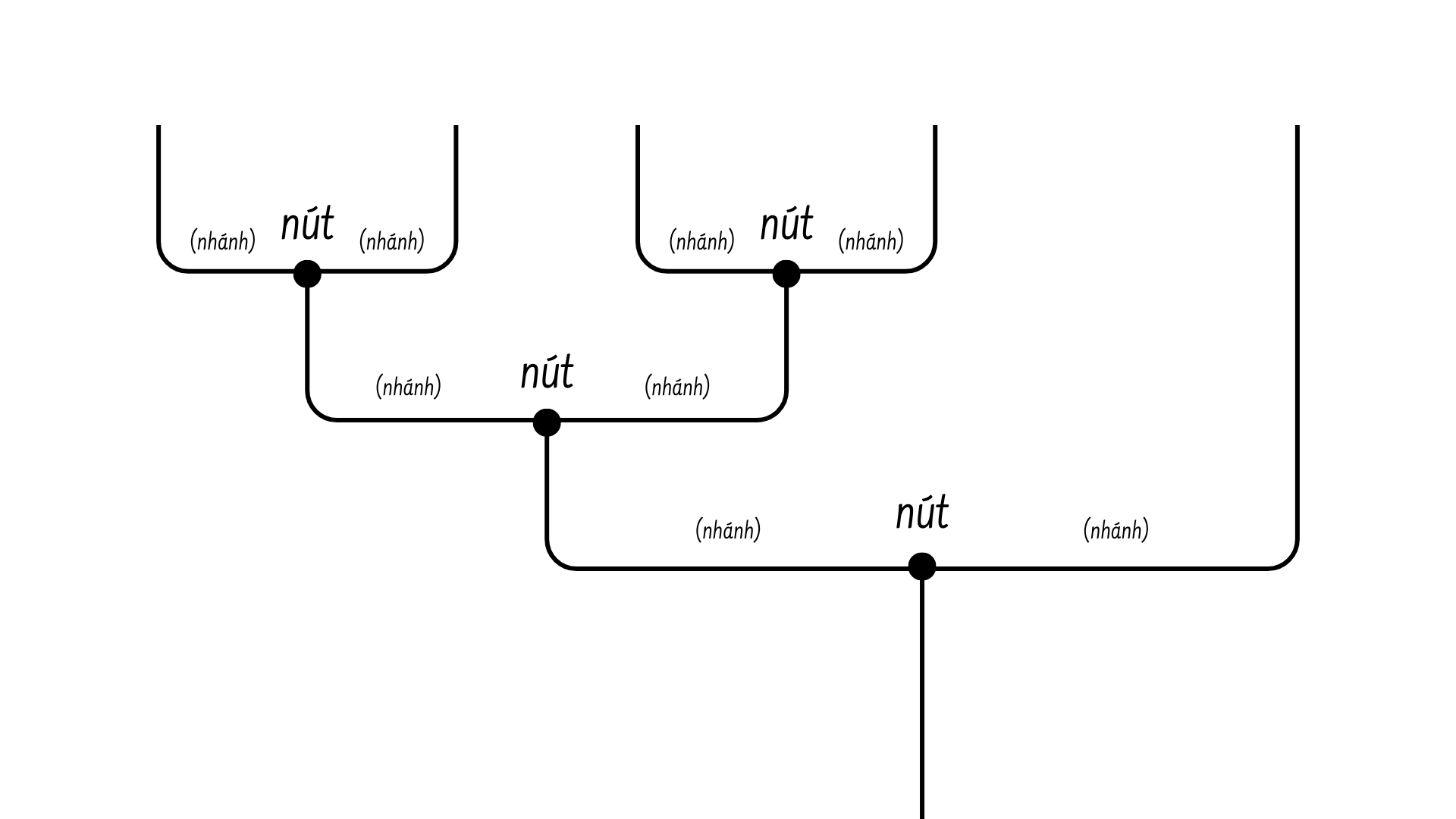
Nhìn chung thì đây là một sơ đồ thể hiện mối quan hệ tiến hóa giữa các loài khác nhau dựa vào các đặc điểm di truyền. Các nút và nhánh biểu thị cho việc các sinh vật trong cùng một loài ban đầu đã tiến hoá theo hai con đường khác nhau để hình thành ra hai loài mới.
2. Hoá học của sự sống
Ở cấp độ cơ bản nhất, sự sống được làm nên bởi các nguyên tố. Có bốn nguyên tố chính thường xuyên xuất hiện bên trong tất cả các sinh vật sống, đó là oxy (O), cacbon (C), hydro (H) và nitơ (N). Và khi so sánh “bộ tứ siêu đẳng” này với “bộ sáu kỳ diệu” đã làm nên đá bazan dưới đáy đại dương và đá granit trên lục địa, chúng ta có thể thấy rằng các sinh vật sống đang sử dụng một tập hợp các nguyên tố hoàn toàn khác (trừ oxy). Tuy nhiên, bất chấp sự khác biệt này, tất cả các nguyên tố trên đều phải tuân theo các định luật hóa học chung nhất.
Nguyên tử và nguyên tố
Và để có thể hiểu được cơ chế hoạt động của các nguyên tố, trước tiên chúng ta sẽ phải đề cập đến các nguyên tử – một đơn vị vật chất nhỏ nhất giữ lại tất cả các tính chất hóa học của nguyên tố đó. Ví dụ, một nguyên tử vàng sẽ mang theo tất cả các tính chất hoá học của vàng. Một đồng xu bằng vàng chỉ đơn giản là chứa một lượng lớn các nguyên tử vàng được đúc lại thành một đồng xu. Chúng ta không thể phân tách các nguyên tử vàng thành bất cứ thứ gì nhỏ hơn mà vẫn giữ được các tính chất của vàng.

Nguyên tử gồm có hai thành phần chính: Nằm ở vùng trung tâm chính là hạt nhân, bao gồm các proton và neutron; còn vùng ngoài cùng của nguyên tử chứa các electron di chuyển liên tục xung quanh hạt nhân.
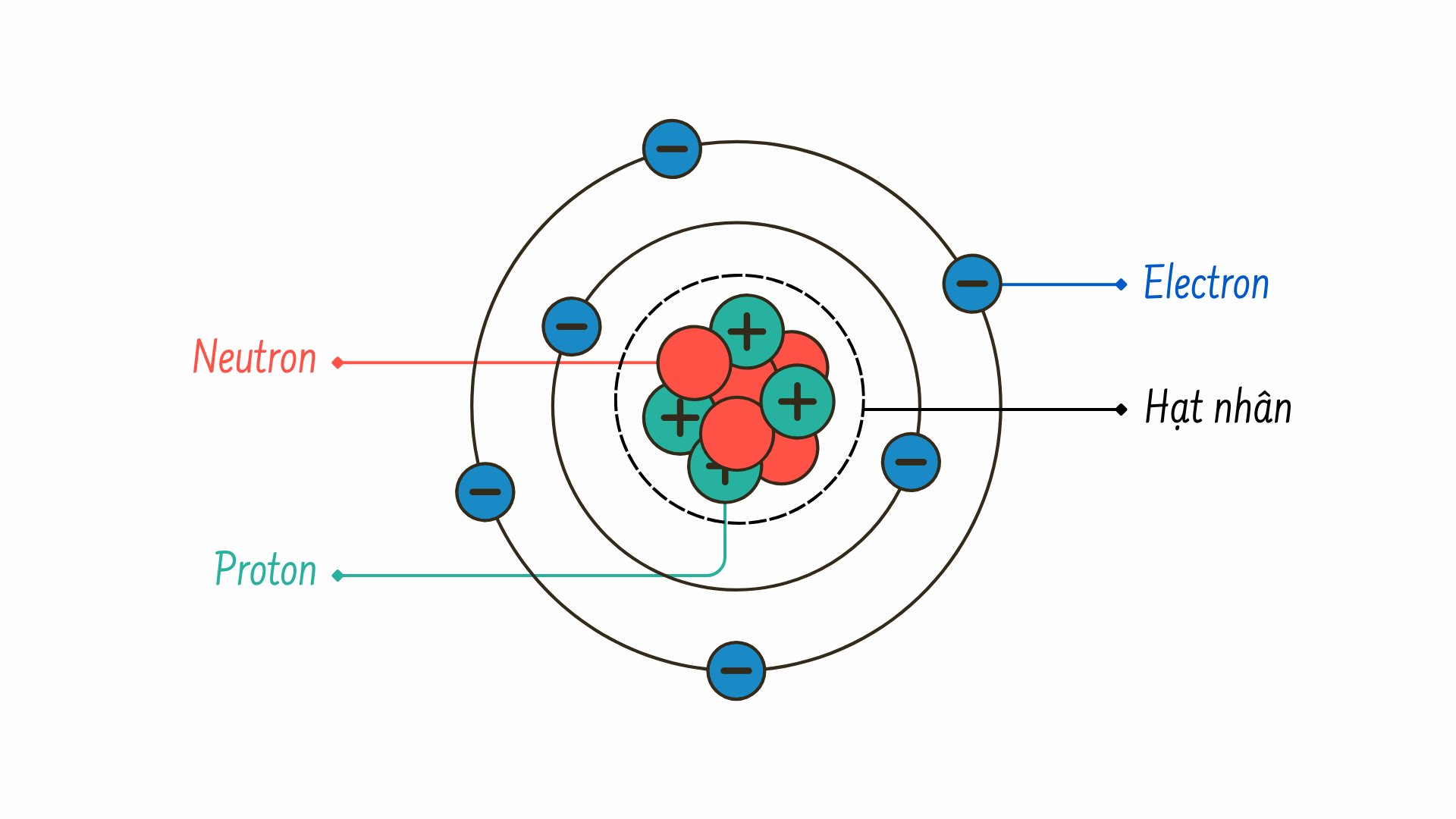
Proton và neutron có khối lượng gần bằng nhau, rơi vào khoảng 1,67 × 10–24 gam. Tuy vậy, điện tích của chúng lại khác nhau: Proton mang điện tích dương còn neutron thì không mang điện tích. Electron có khối lượng nhỏ hơn nhiều so với proton, chỉ nặng khoảng 9,11 × 10–28 gam (nhỏ hơn 10.000 lần). Vì vậy, khi xem xét khối lượng của nguyên tử, chúng ta thường bỏ qua khối lượng của electron và tính toán khối lượng của nguyên tử dựa trên số lượng proton và neutron của nó mà thôi.
Mặc dù không có đóng góp đáng kể nào vào khối lượng nhưng tầm ảnh hưởng của electron đối với điện tích tổng thể của nguyên tử lại rất lớn. Trong các nguyên tử trung tính, số electron di chuyển xung quanh hạt nhân bằng với số proton bên trong hạt nhân, dẫn đến nguyên tử được trung hoà về điện.
Khi chúng ta xét đến kích thước của proton, neutron và electron, phần lớn thể tích của các nguyên tử (khoảng 99%) là không gian trống. Vậy thì tại sao các nguyên tử lại không đi xuyên qua nhau? Đó là bởi các electron di chuyển nhanh đến nỗi chúng có thể tạo thành một “lớp màng” điện tích âm xung quanh nguyên tử, từ đó chúng sẽ đẩy các “lớp màng” của các nguyên tử khác ra xa.
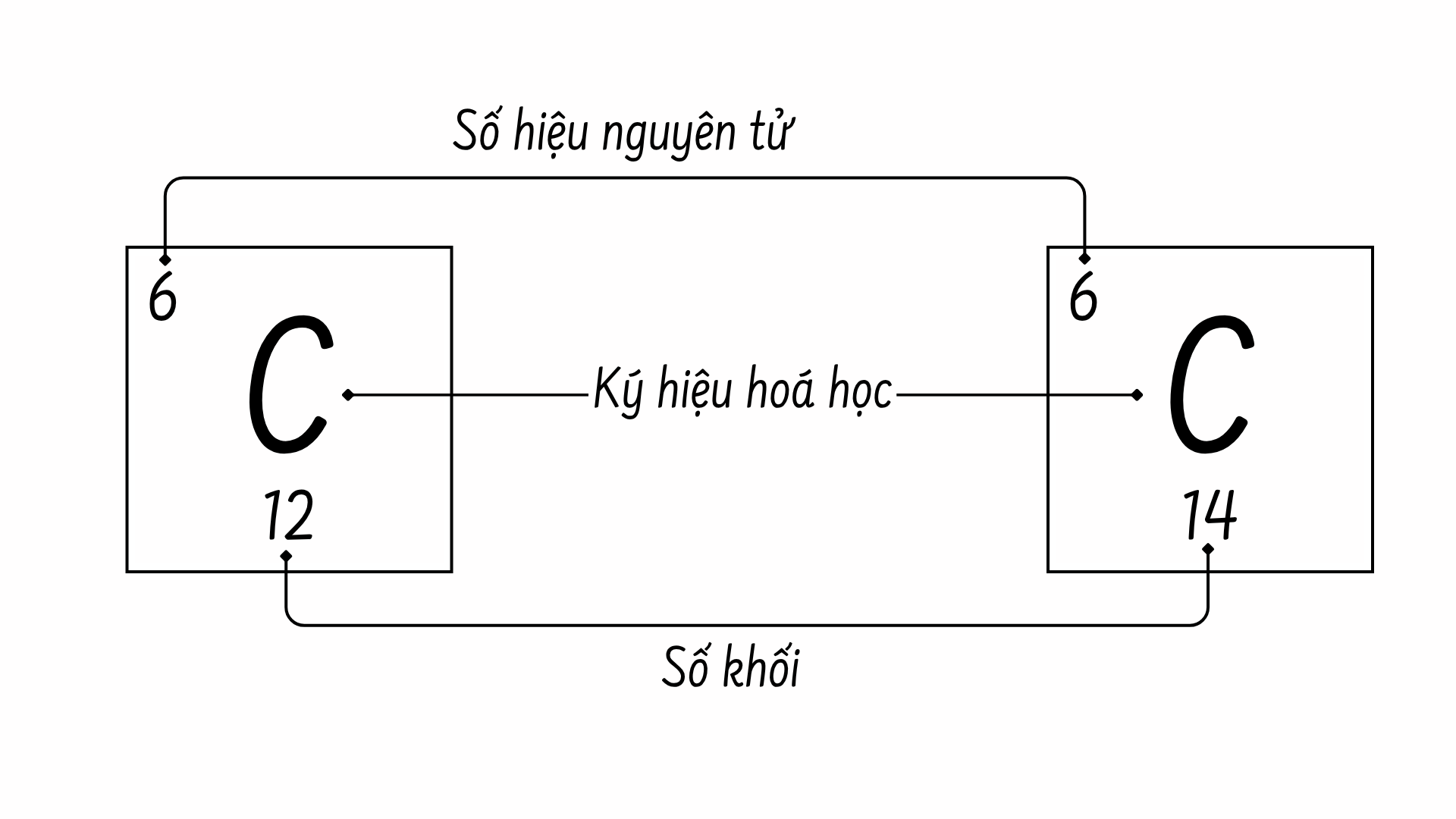
Các nguyên tử bên trong mỗi nguyên tố đều chứa một lượng proton và electron khác nhau. Và số lượng của proton sẽ quyết định số hiệu nguyên tử của nguyên tố – một con số dùng để phân biệt các nguyên tố này so với các nguyên tố khác. Tuy nhiên, số lượng neutron có thể thay đổi, dẫn đến sự hình thành của các đồng vị – một tập hợp các “phiên bản” khác nhau của cùng một nguyên tử do có sự khác biệt về số lượng neutron mà chúng sở hữu.
Cùng nhau, số lượng proton và neutron sẽ quyết định số khối của nguyên tố. Và vì các đồng vị của một nguyên tố sẽ có số khối hơi khác nhau, người ta đã xác định khối lượng nguyên tử là giá trị trung bình thu được sau khi tính toán khối lượng nguyên tử của các đồng vị tự nhiên. Thông thường, con số thu được sẽ là một phần thập phân. Ví dụ, khối lượng nguyên tử của cacbon (C) là 12,011 vì clo được cấu tạo từ một số đồng vị, bao gồm 12C (6 protons và 6 neutrons) là phổ biến nhất, sau đó là 13C (6 protons và 7 neutrons) và 14C (6 protons và 8 neutrons)
Đồng vị phóng xạ
Một số đồng vị có thể phát ra neutron, proton và electron rồi sau đó đạt được một cấu hình nguyên tử ổn định hơn. Đây được gọi là các đồng vị phóng xạ (radioisotope). Sau đây là một ví dụ về 14C.
Cacbon thường tồn tại trong bầu khí quyển dưới dạng cacbon dioxit (CO2) và metan (CH4). Cacbon-14 (14C) là một đồng vị phóng xạ tự nhiên được tạo ra trong bầu khí quyển bằng cách kết hợp 14N với một neutron và mất đi một proton do va chạm với các tia vũ trụ.
14N + neutron → 14C + proton
Khi một sinh vật sống hấp thụ 14C ban đầu dưới dạng cacbon dioxit trong quá trình quang hợp, nồng độ 14C bên trong cơ thể nó bằng với nồng độ ¹⁴C trong bầu khí quyển. Khi một sinh vật chết đi, nó sẽ không hấp thụ 14C nữa , vì vậy tỷ lệ giữa 14C và 12C sẽ giảm đi khi 14C phân rã thành 14N trong một quá trình được gọi là phân rã beta – chúng sẽ phát ra electron hoặc positron.
14C → 14N + electron + positron
Sau khoảng 5.730 năm, một nửa lượng 14C ban đầu sẽ được chuyển hóa trở lại thành 14N ổn định hơn. Và khoảng thời gian này được gọi là chu kỳ bán rã. Bởi vì chu kỳ bán rã của 14C khá dài nên các nhà khoa học sử dụng nó để xác định tuổi của các vật thể như xương hoặc gỗ cổ.
Bằng cách so sánh tỷ lệ 14C/12C bên trong một vật thể với tỷ lệ 14C/12C trong bầu khí quyển, các nhà khoa học có thể xác định được tuổi của một mẫu vật nếu nó không quá 50.000 năm. Mỗi một nguyên tố sẽ có các đồng vị với chu kỳ bán rã khác nhau. Ví dụ, 40K (kali-40) có chu kỳ bán rã là 1,25 tỷ năm và 235U (urani-235) có chu kỳ bán rã là 700 triệu năm.
Thông qua việc sử dụng phương pháp định tuổi bằng các đồng vị phóng xạ, các nhà khoa học có thể xác định được tuổi của các loại hóa thạch hoặc các mẫu vật khác của các loài sinh vật đã tuyệt chủng để hiểu được cách các loài sinh vật này đã tiến hóa như thế nào từ các loài trước đó.
Mô hình Bohr
Như chúng ta đã đề cập đến trong bài viết về quang phổ, năm 1913, nhà khoa học người Đan Mạch Niels Bohr đã phát triển ra một mô hình nguyên tử. Ông đề xuất rằng electron chỉ có thể di chuyển trong một vài quỹ đạo (orbital) nhất định. Một electron thường tồn tại trong quỹ đạo có năng lượng thấp nhất (gần hạt nhân nhất). Nếu electron này hấp thu năng lượng từ một photon ánh sáng, nó sẽ được đẩy lên lớp vỏ có năng lượng cao hơn. Tuy nhiên, electron ở trạng thái kích thích này lại không ổn định và sẽ nhanh chóng phân rã trở lại trạng thái cơ bản. Trong quá trình đó, nó sẽ phát ra một photon ánh sáng.
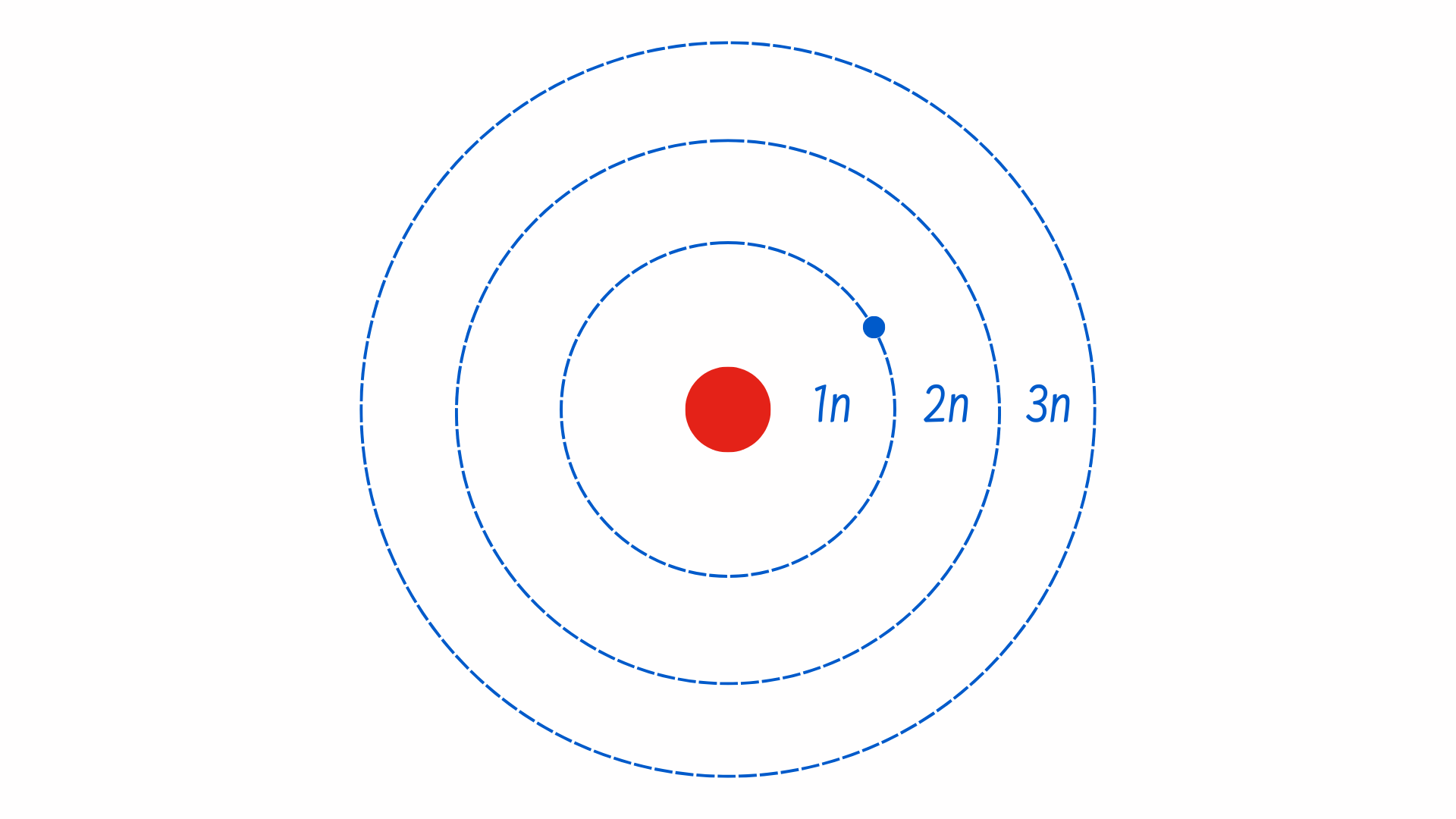
Các electron lấp đầy các quỹ đạo theo một trình tự nhất quán: chúng sẽ lấp đầy các quỹ đạo gần hạt nhân trước (có mức năng lượng thấp), sau đó tiếp tục lấp đầy các quỹ đạo ở xa hạt nhân hơn (có mức năng lượng cao). Các electron ở quỹ đạo ngoài cùng quyết định mức độ ổn định năng lượng của nguyên tử và sẽ tạo liên kết hóa học với các nguyên tử khác để tạo thành phân tử.
Trong các điều kiện bình thường, các nguyên tử sẽ lấp đầy các lớp electron bên trong trước, từ đó dẫn đến số lượng electron ở lớp ngoài cùng sẽ bị thay đổi. Lớp electron trong cùng có tối đa 2 electron hóa trị (là các electron nằm ở lớp vỏ ngoài cùng của nguyên tử, giúp hình thành nên các liên kết hóa học và quyết định mức độ ổn định của một nguyên tố) nhưng hai lớp electron tiếp theo có thể “dung chứa” tới 8 electron hóa trị. Đây được gọi là quy tắc bát tử – một quy tắc phát biểu rằng các nguyên tử sẽ ổn định hơn về mặt năng lượng khi chúng có 8 electron trong lớp electron ngoài cùng (hay lớp electron hoá trị). Và con số 8 này chỉ là một trong số các “con số kỳ diệu” khác như 2, 10 hoặc 18.
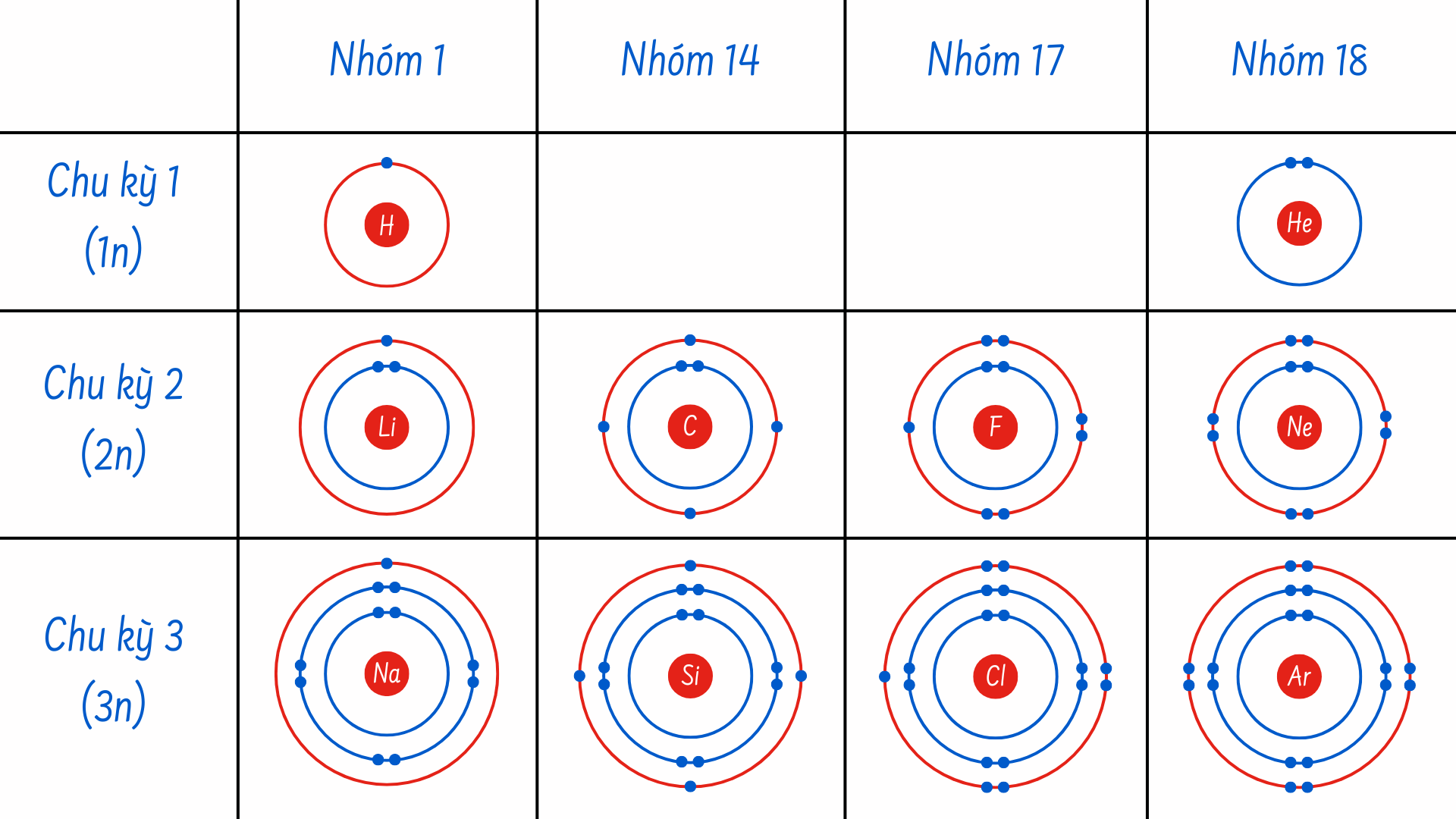
Như vậy, khi xem xét lại bảng tuần hoàn hoá học, chúng ta có thể thấy rằng các nguyên tố đang được sắp xếp dựa trên trên số proton (và electron), từ đó chúng ta có thể dễ dàng biết được số lượng và vị trí của các electron.
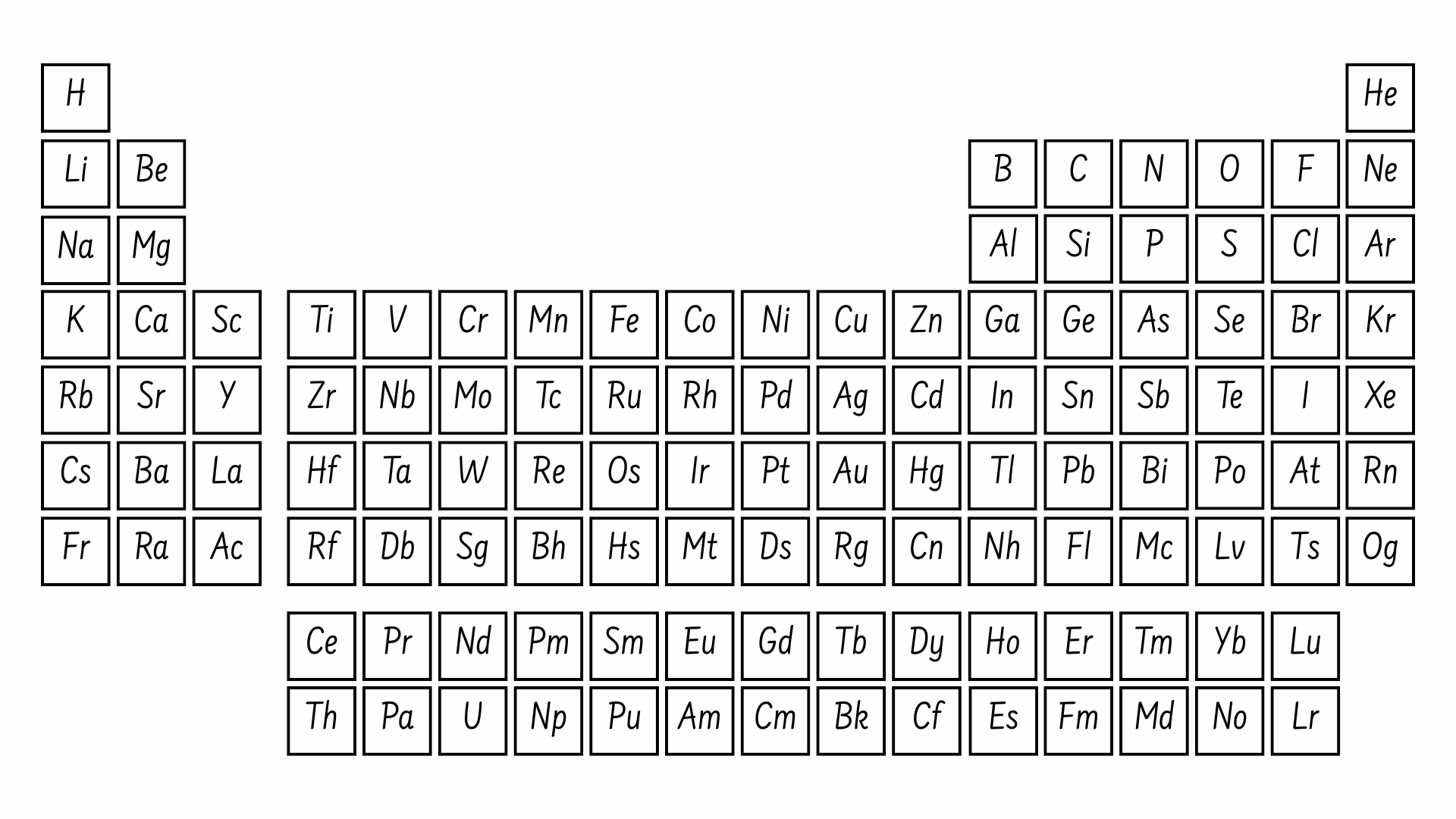
Hãy bắt đầu với một số nguyên tố ở cột ngoài cùng bên phải. Các nguyên tử nhóm 18 là heli (He), neon (Ne) và argon (Ar) đều có lớp electron ngoài cùng đã được lấp đầy, do đó chúng sẽ không cần phải chia sẻ electron với các nguyên tử khác để đạt được trạng thái ổn định. Do không có sự chia sẻ electron nên chúng sẽ không hình thành liên kết với các nguyên tử khác – tức là không phản ứng và chúng được gọi là khí hiếm (trơ về mặt hoá học).
Đối với các nguyên tố nhóm 1 ở cột bên trái, chẳng hạn như hydro (H), liti (Li) và natri (Na), chúng đều có 1 electron ở lớp vỏ ngoài cùng. Điều đó có nghĩa là chúng có thể đạt được cấu hình ổn định (tức là lớp vỏ ngoài cùng được lấp đầy) bằng cách chia sẻ hoặc cho đi 1 electron. Hydro sẽ chia sẻ electron của nó để đạt được cấu hình này, trong khi liti và natri sẽ cho đi 1 electron của chúng để trở nên ổn định hơn. Khi cho đi 1 electron mang điện tích âm, chúng sẽ trở thành các ion mang điện tích dương.
Các nguyên tố nhóm 17, bao gồm flo và clo, có 7 electron ở lớp vỏ ngoài cùng, vì vậy chúng có xu hướng lấp đầy lớp vỏ này bằng cách “lấy đi” một electron từ các nguyên tử hoặc phân tử khác, khiến chúng trở thành các ion mang điện tích âm.
Quỹ đạo electron
Mặc dù khá hữu ích trong việc giải thích cơ chế phản ứng và liên kết hóa học của một số nguyên tố, mô hình Bohr lại không phản ánh chính xác cách mà các electron phân bố trong không gian xung quanh hạt nhân. Chúng không quay quanh hạt nhân như Trái Đất quay quanh Mặt Trời mà chúng thường có các quỹ đạo (orbital).
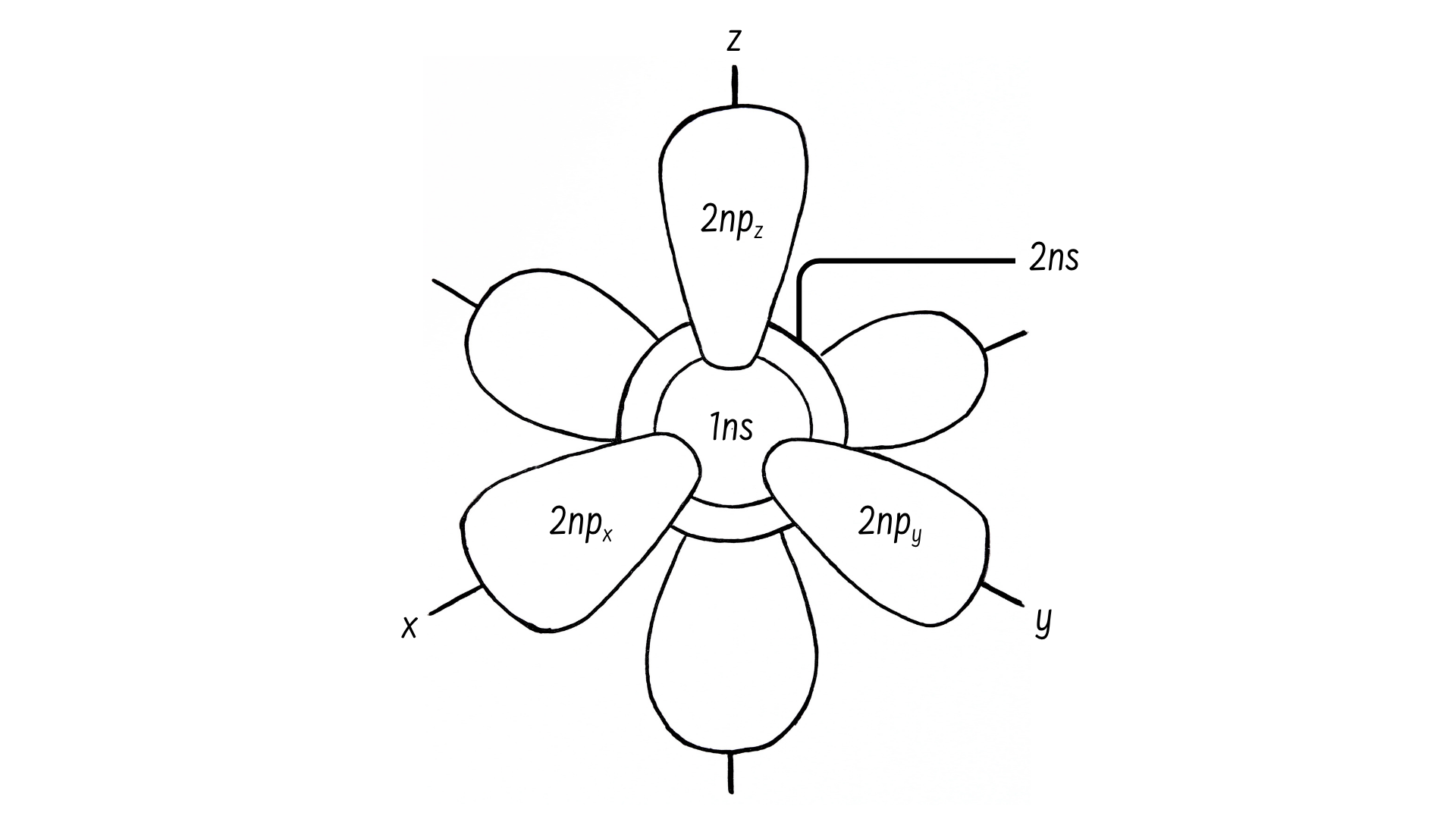
Những hình dạng tương đối phức tạp này là kết quả của việc electron không chỉ hoạt động giống như hạt mà chúng còn có thể hoạt động giống như sóng. Và để biểu thị đặc tính này, cơ học lượng tử đã đưa ra một hàm sóng nhằm thể hiện xác suất về vị trí của một electron tại một thời điểm nhất định. Và vùng không gian mà chúng ta có thể dễ dàng tìm thấy một electron (xác suất cao) được gọi là quỹ đạo của nó.
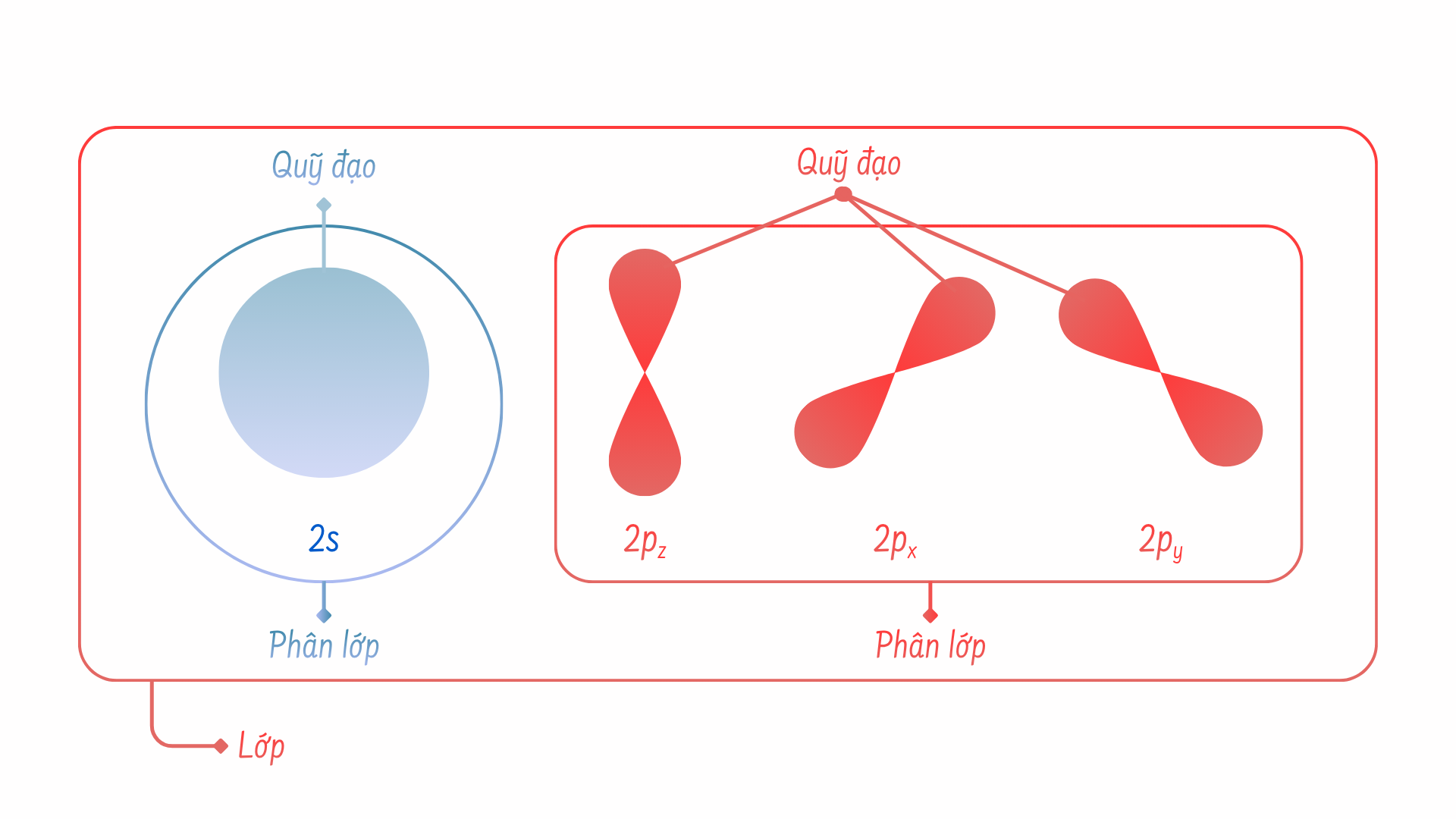
Hãy nhớ rằng mô hình Bohr bên trên đã mô tả các lớp electron của nguyên tử. Và trong mỗi lớp electron này sẽ có các phân lớp (s, p, d, f) và mỗi phân lớp sẽ có một số lượng quỹ đạo nhất định. Mặc dù không thể tính toán chính xác vị trí của một electron, các nhà khoa học biết rằng rất có thể nó sẽ nằm ở trong các quỹ đạo này.
Phân lớp s sẽ có hình cầu và một orbital. Lớp chính 1n chỉ có một quỹ đạo s duy nhất (có thể chứa nhiều nhất 2 electron). Lớp chính 2n có một phân lớp s và một phân lớp p (có thể chứa nhiều nhất 8 electron). Phân lớp p có ba quỹ đạo hình quả tạ.
Lớp chính 3n có các phân lớp s, p và d (có thể chứa nhiều nhất 18 electron). Lớp chính 4n có các obitan s, p, d và f (có thể chứa 32 electron). Các phân lớp d và f có hình dạng phức tạp hơn và lần lượt có năm và bảy quỹ đạo. Càng ở xa hạt nhân, số lượng electron và mức năng lượng sẽ ngày càng tăng.
Quỹ đạo gần hạt nhân nhất (orbital 1s) có thể chứa tối đa 2 electron. Quỹ đạo này tương đương với lớp electron trong cùng của mô hình Bohr. Quỹ đạo 1s là quỹ đạo gần hạt nhân nhất và luôn được lấp đầy trước tiên. Hydro có một electron; do đó, nó chỉ chiếm một vị trí trong orbital 1s, ký hiệu là 1s1. Heli có 2 electron; do đó nó có thể lấp đầy orbital 1s với hai electron, ký hiệu là 1s2. Trong bảng tuần hoàn hoá học, hydro và heli là hai nguyên tố duy nhất trong hàng đầu tiên (hay chu kỳ đầu tiên). Điều này là do chúng chỉ có electron trong lớp vỏ đầu tiên, orbital 1s. Hydro và heli là hai nguyên tố chỉ có duy nhất orbital 1s và không có orbital nào khác.
Lớp electron thứ hai có thể chứa tối đa là 8 electron. Lớp này chứa một orbital s hình cầu và ba orbital p hình “quả tạ”, mỗi orbital chứa hai electron. Sau khi orbital 1s được lấp đầy, lớp electron thứ hai sẽ được lấp đầy, trước tiên nó sẽ lấp đầy orbital 2s và sau đó là ba orbital p. Khi lấp đầy các orbital p, mỗi orbital sẽ lần lượt nhận được 1 electron. Sau khi mỗi orbital p đã có được 1 electron, nó sẽ bắt đầu nhận thêm electron thứ hai.
Chẳng hạn, Liti (Li) có 3 electron. Hai electron sẽ lấp đầy orbital 1s trước và electron thứ ba sẽ lấp đầy orbital 2s. Cấu hình electron của nó sẽ là 1s2 2s1. Ngược lại, neon (Ne) có tổng cộng 10 electron: 2 electron nằm trong orbital 1s và 8 electron lấp đầy lớp thứ hai (hai electron trong orbital 2s và sáu electron trong orbital 2p). Do đó, nó là một khí trơ, ổn định về mặt năng lượng và hiếm khi tạo ra các liên kết hóa học với các nguyên tử khác.
Liên kết hoá học
Như vậy, tất cả các nguyên tố đều trở nên ổn định hơn khi lớp vỏ ngoài cùng của chúng tuân theo quy tắc bát tử. Tuy nhiên, không phải lúc nào các electron cũng trôi nổi tự do và chỉ chờ các nguyên tử đến “chiếm lấy”. Để có thể lấp đầy lớp vỏ ngoài cùng, các nguyên tử hình thành liên kết hóa học với các nguyên tử khác để thu nhận các electron cần thiết nhằm đạt được cấu hình electron ổn định nhất. Khi hai hay nhiều nguyên tử liên kết hóa học với nhau, cấu trúc hóa học thu được là một phân tử. Các nguyên tử có thể tạo thành phân tử bằng cách cho, nhận hoặc chia sẻ electron để lấp đầy lớp vỏ ngoài cùng của chúng.
Một số nguyên tử trở nên ổn định hơn khi chúng tiếp nhận hoặc mất đi một (hoặc nhiều) electron và tạo thành các ion. Cơ chế này giúp lấp đầy lớp electron ngoài cùng và làm cho chúng ổn định hơn về mặt năng lượng. Vì số electron không bằng số proton nên mỗi ion sẽ mang theo một điện tích. Cation là các ion dương được hình thành bằng cách cho đi electron. Anion là các ion âm được hình thành bằng cách nhận thêm electron.
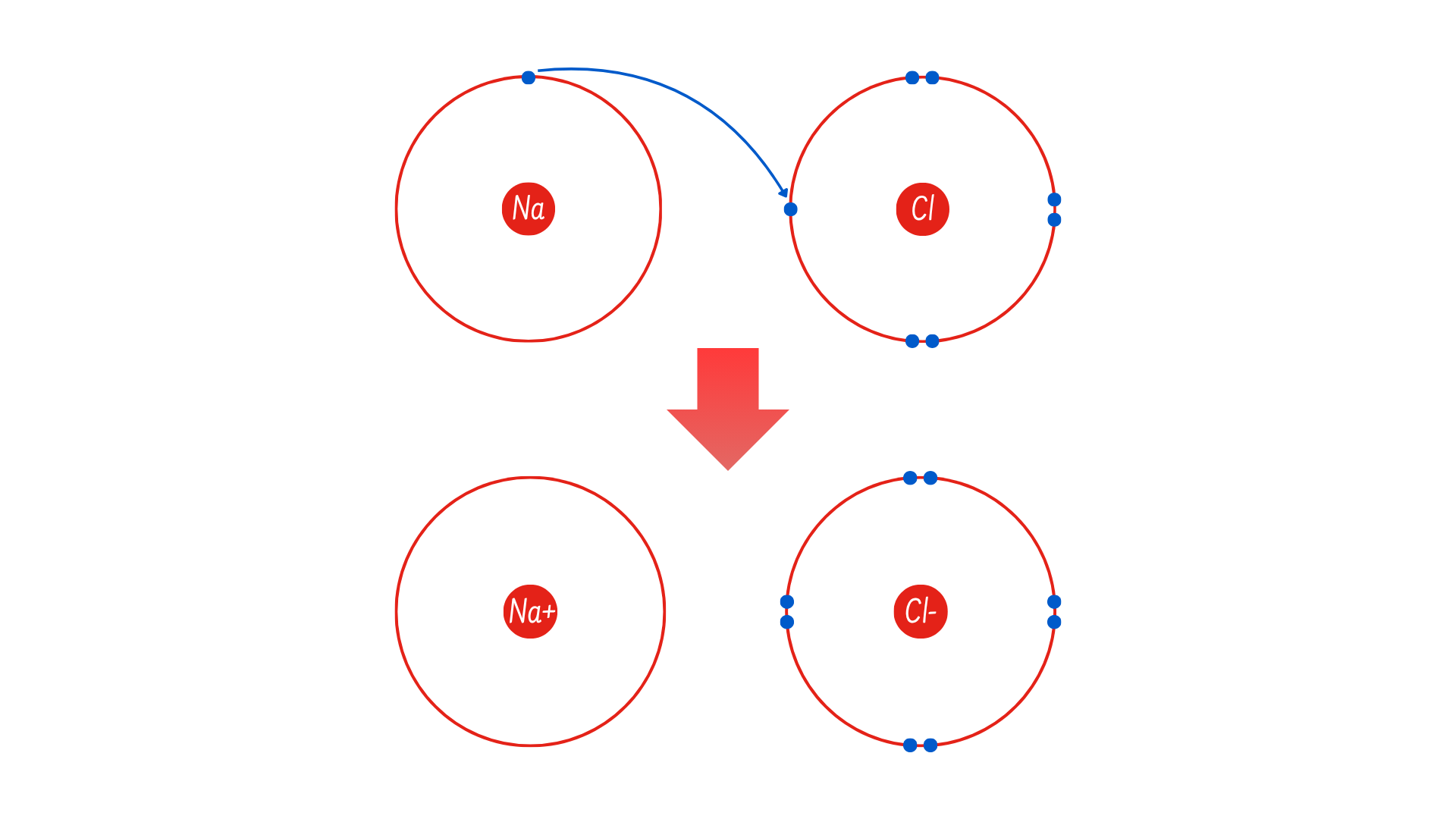
Ví dụ, natri (Na) chỉ có một electron ở lớp vỏ ngoài cùng. Việc natri cho đi 1 electron sẽ tốn ít năng lượng hơn so với việc nhận thêm 7 electron để lấp đầy lớp vỏ ngoài cùng. Nếu natri mất đi một electron, nó sẽ có 11 proton, 11 neutron và chỉ còn 10 electron, mang điện tích là +1. Lúc này chúng ta gọi nó là ion natri.
Clo (Cl) ở trạng thái cơ bản thường có 7 electron ở lớp vỏ ngoài cùng. Một lần nữa, việc clo nhận thêm 1 electron sẽ hiệu quả hơn về mặt năng lượng so với việc phải cho đi tận 7 electron. Do đó, nó có xu hướng nhận thêm 1 electron để tạo ra một ion có 17 proton, 17 neutron và 18 electron, mang điện tích là –1. Lúc này chúng ta gọi nó là ion clorua.
Trong ví dụ này, natri sẽ nhường đi 1 electron và clo sẽ tiếp nhận electron đó để lấp đầy lớp vỏ của nó. Cả hai ion giờ đây đều đã thỏa mãn quy tắc bát tử và có lớp vỏ ngoài cùng rất hoàn chỉnh, đồng thời hai ion mang điện tích trái dấu này đã hình thành nên một liên kết ion để tạo thành tinh thể natri clorua (hay muối ăn) trung hòa về điện.
Một cách khác để thỏa mãn quy tắc bát tử là các nguyên tử có thể chia sẻ electron để tạo thành liên kết cộng hóa trị. Chúng ta thường thấy liên kết cộng hóa trị trong các phân tử hữu cơ, chẳng hạn như DNA và protein của chúng ta. Chúng ta cũng có thể tìm thấy liên kết cộng hóa trị trong các phân tử vô cơ như H2O, CO2 và O2. Các liên kết này có thể chia sẻ 1, 2 hoặc 3 cặp electron để tạo thành liên kết đơn, đôi và ba tương ứng. Càng nhiều liên kết cộng hóa trị, liên kết giữa hai nguyên tử càng mạnh. Do đó, liên kết ba là liên kết mạnh nhất.
Độ bền của các liên kết cộng hóa trị là một trong những lý do chính khiến cho các sinh vật sống gặp rất nhiều khó khăn trong việc thu nhận nitơ để xây dựng nên các phân tử lớn hơn, mặc dù nitơ (N2) là loại khí dồi dào nhất trong bầu khí quyển. Phân tử nitơ bao gồm hai nguyên tử nitơ hình thành liên kết ba với nhau. Và việc chia sẻ 3 cặp electron này cho phép hai nguyên tử nitơ lấp đầy lớp vỏ electron ngoài cùng của chúng, từ đó làm cho phân tử trở nên ổn định hơn và rất khó có thể bị phá vỡ.
Có hai loại liên kết cộng hóa trị chính: phân cực và không phân cực. Trong liên kết cộng hóa trị phân cực, electron không được chia sẻ một cách đồng đều vì chúng bị hút mạnh hơn về một phía của nguyên tử này so với nguyên tử kia. Do sự phân bố không đồng đều này, các đầu mang điện tích dương nhẹ (δ+) hoặc âm nhẹ (δ–) sẽ được hình thành.
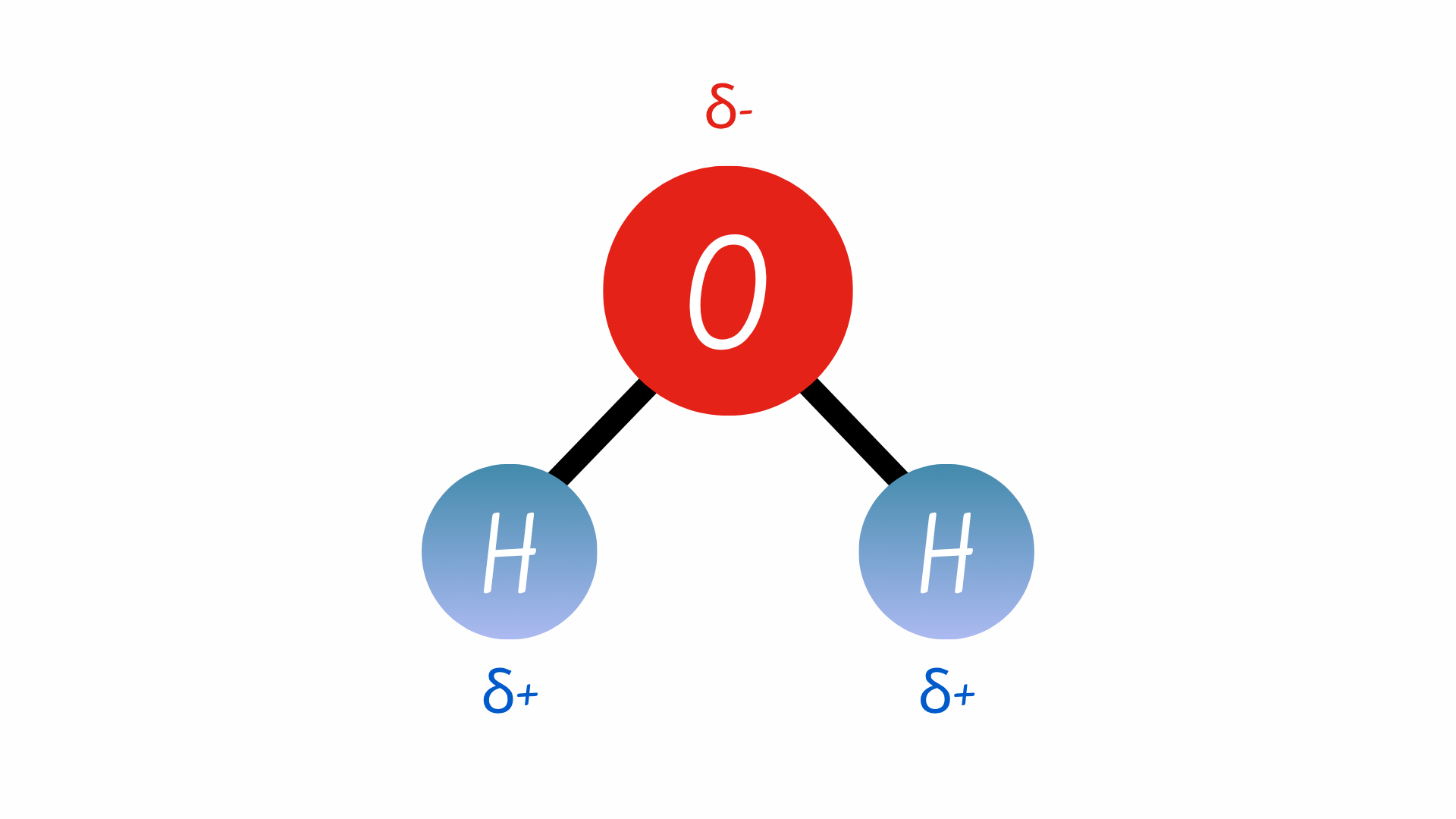
Ở hình ảnh trên, nước là một phân tử phân cực, trong đó các nguyên tử hydro mang điện tích dương một phần và các nguyên tử oxy mang điện tích âm một phần. Điều này xảy ra là do lực hút electron của hạt nhân oxy mạnh hơn so với lực hút electron của hạt nhân hydro. Do đó, oxy có độ âm điện cao hơn so với hydro và các electron dùng chung “dành nhiều thời gian” hơn ở gần hạt nhân oxy so với hạt nhân của nguyên tử hydro, từ đó làm cho các nguyên tử oxy và hydro mang điện tích âm và dương nhẹ tương ứng.
Liên kết cộng hóa trị không phân cực hình thành giữa hai hay nhiều nguyên tử có sự chia sẻ electron đồng đều. Ví dụ, metan (CH4) bao gồm cacbon có 4 electron ở lớp vỏ ngoài cùng và cần thêm bốn electron nữa để đạt tới con số 8 “kỳ diệu”. Và nó thu nhận thêm 4 electron này từ 4 nguyên tử hydro – mỗi nguyên tử cung cấp thêm 1 electron, tạo thành một lớp vỏ ngoài ổn định bao gồm 8 electron. Bên cạnh đó, mỗi nguyên tử hydro cũng cần thêm 1 electron cho lớp vỏ ngoài cùng của nó để tiến tới con số 2 “kỳ diệu”. Lúc này, các nguyên tử đã chia sẻ các electron một cách rất đồng đều và đã tạo ra một phân tử cộng hóa trị không phân cực.
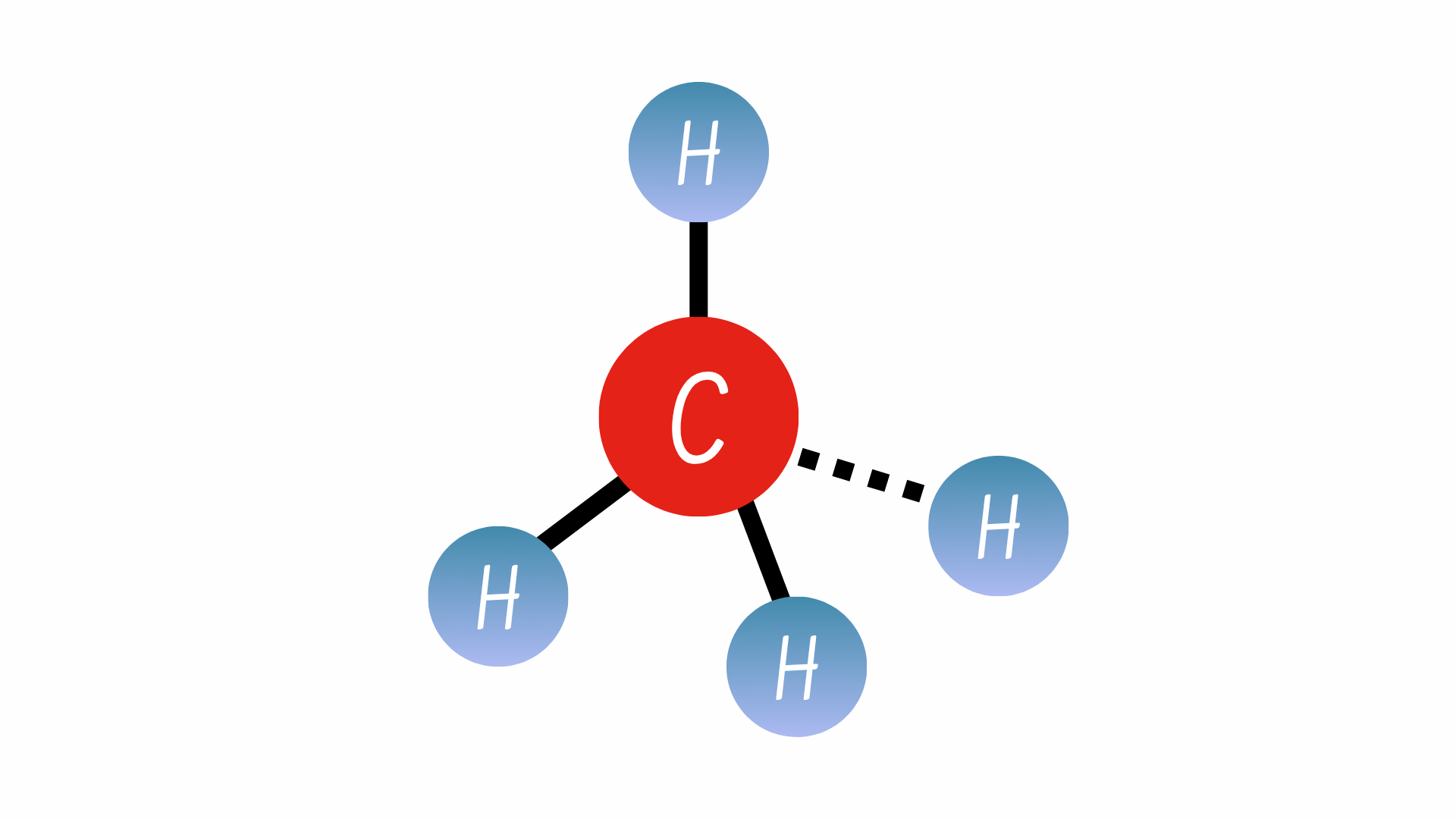
Tuy nhiên, không phải liên kết nào cũng đều là liên kết ion hoặc liên kết cộng hóa trị. Các liên kết yếu hơn cũng có thể được hình thành giữa các phân tử. Và hai loại liên kết thường gặp nhất chính là liên kết hydro và liên kết van der Waals. Nếu không có hai loại liên kết này, sự sống sẽ không thể tồn tại.
Như đã phân tích ở bên trên, khi các liên kết cộng hóa trị phân cực chứa hydro hình thành, hydro trong liên kết đó sẽ mang điện tích dương nhẹ. Lúc này, nó sẽ bị hút bởi các điện tích âm lân cận. Khi điều này xảy ra, một liên kết yếu sẽ được hình thành giữa điện tích δ+ của hydro ở phân tử này và điện tích δ– của phân tử khác, thường là oxy. Và đây là một liên kết hydro – loại liên kết thường xuyên xảy ra giữa các phân tử nước.
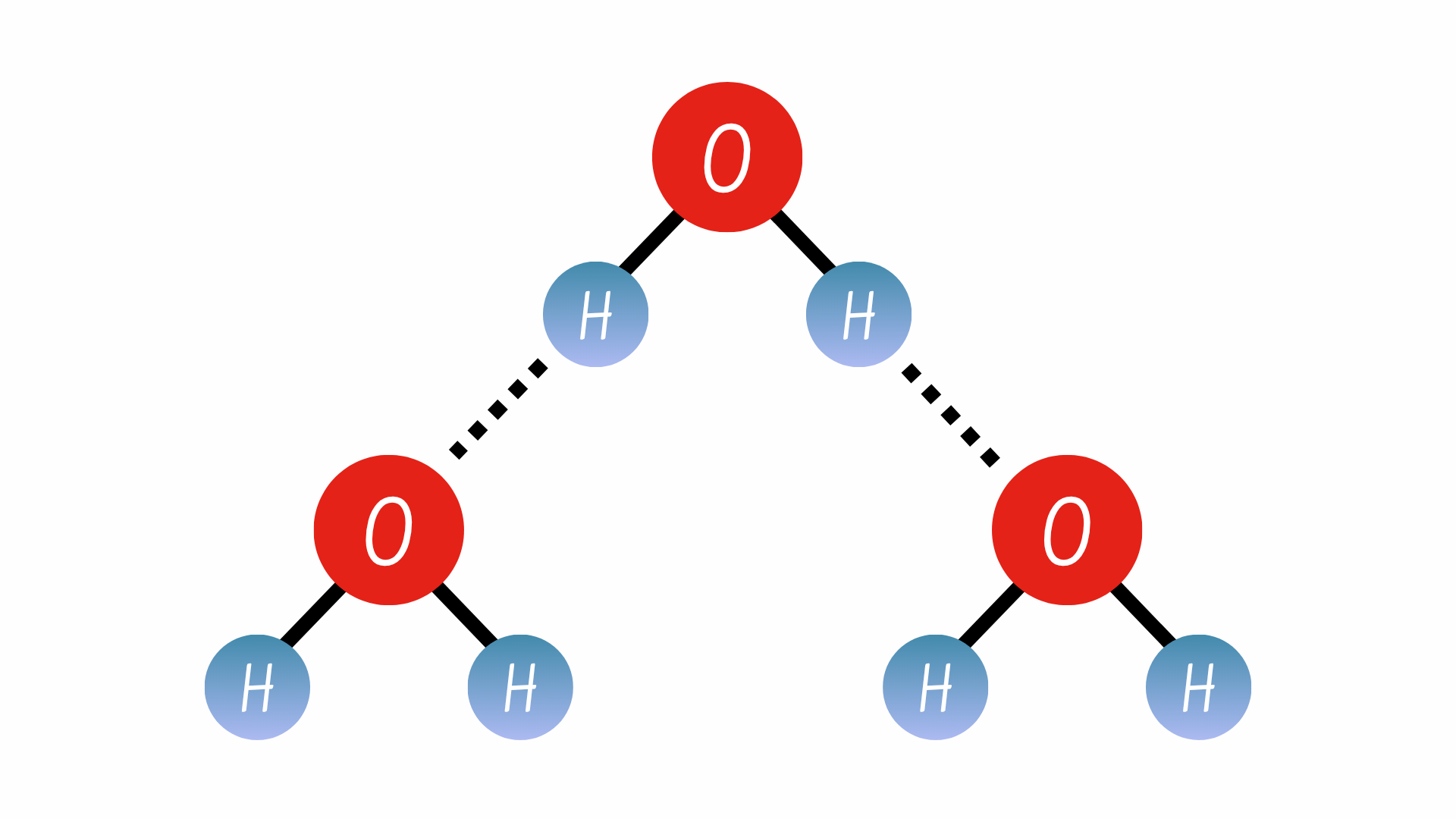
Bên cạnh liên kết hydro, liên kết van der Waals lại có thể xảy ra giữa bất kỳ hai hay nhiều phân tử nào và phụ thuộc vào sự dao động rất nhỏ trong mật độ electron. Để lực hút này có thể xảy ra, các phân tử phải ở rất gần nhau.
Như vậy, những liên kết này – cùng với liên kết ion, liên kết cộng hóa trị và liên kết hydro – đã góp phần tạo nên những cấu trúc sinh học ngày càng phức tạp và đa dạng hơn trên Trái Đất.
3. Cacbon – “Xương sống” của “sự sống”
Trong sinh học có rất nhiều các phân tử phức tạp được gọi là đại phân tử, chẳng hạn như protein, axit nucleic (RNA và DNA), carbohydrate và lipid, đặc biệt quan trọng đối với sự sống. Và thành phần cơ bản nhất của tất cả các đại phân tử này chính là cacbon – những nguyên tử có những đặc tính rất độc đáo cho phép nó tạo ra liên kết cộng hóa trị với tối đa bốn nguyên tử khác, trở thành một lựa chọn rất lý tưởng để làm nên “xương sống” của các đại phân tử.
Hydrocarbon
Các nguyên tử cacbon riêng lẻ có lớp electron ngoài cùng chưa được hoàn chỉnh. Với số hiệu nguyên tử là 6 (sáu electron và sáu proton), hai electron đầu tiên lấp đầy lớp electron bên trong, để lại bốn electron ở lớp thứ hai. Do đó, các nguyên tử cacbon có thể tạo ra tối đa bốn liên kết cộng hóa trị với các nguyên tử khác để thỏa mãn quy tắc bát tử. Phân tử metan là một ví dụ rất điển hình: nó có công thức hóa học là CH4 với mỗi nguyên tử hydro tạo thành một liên kết cộng hóa trị đơn với nguyên tử cacbon bằng cách dùng chung một cặp electron. Và nhờ vào các đặc tính này, cacbon đã tạo nên một “nền móng” vô cùng vững chắc giúp xây dựng nên các phân tử hữu cơ có cấu trúc phức tạp hơn.
Hydrocarbon là các phân tử hữu cơ chỉ bao gồm cacbon và hydro. Chúng ta thường sử dụng hợp chất này rất nhiều trong cuộc sống hàng ngày, chẳng hạn như propan trong bếp ga hoặc butan trong bật lửa. Các liên kết cộng hóa trị giữa các nguyên tử trong hydrocarbon lưu trữ một lượng năng lượng khổng lồ, được giải phóng khi các phân tử này bốc cháy (hay oxy hóa). Thực chất, metan (CH4) là một phân tử hydrocarbon đơn giản nhất với một nguyên tử cacbon ở trung tâm liên kết với bốn nguyên tử hydro khác, tạo thành một hình tứ diện với bốn mặt tam giác.

Là xương sống của các đại phân tử bên trong các sinh vật sống, hydrocarbon có thể tồn tại dưới dạng chuỗi, vòng hoặc cả hai. Hơn nữa, các liên kết cacbon-cacbon riêng lẻ có thể là liên kết cộng hóa trị đơn, đôi hoặc ba, và mỗi loại liên kết sẽ ảnh hưởng đến cấu trúc hình học của các phân tử theo một cách rất cụ thể. Và cấu trúc hình học ba chiều này của các đại phân tử là vô cùng quan trọng đối với cách chúng tương tác và hoạt động.
Các liên kết nối tiếp giữa các nguyên tử cacbon sẽ tạo thành chuỗi hydrocarbon. Các liên kết đôi và liên kết ba sẽ có khả năng làm thay đổi hình dạng của phân tử: liên kết đơn cho phép quay quanh trục của liên kết; trong khi liên kết đôi dẫn đến cấu hình phẳng và liên kết ba dẫn đến cấu hình tuyến tính.
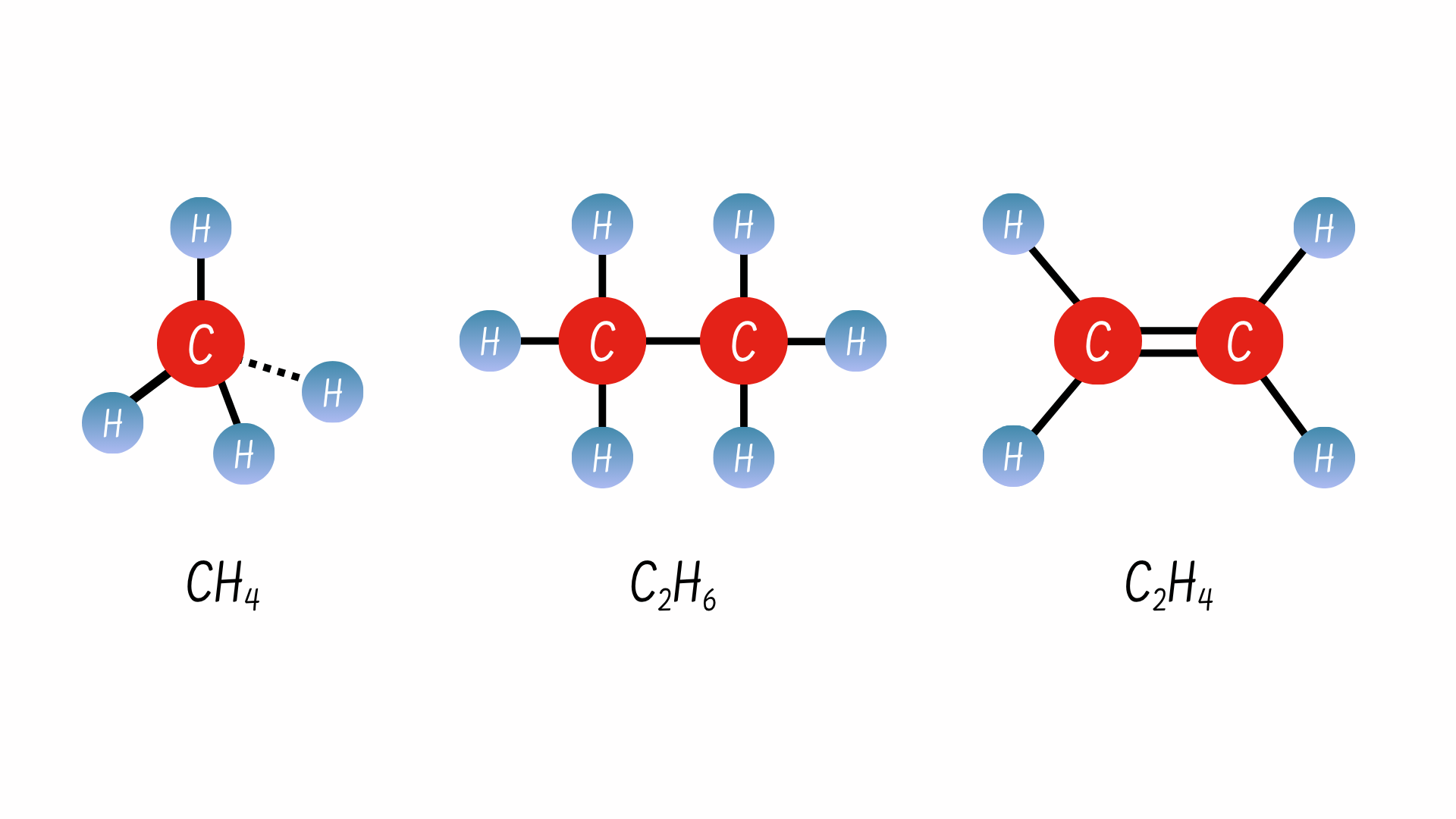
Cho đến nay, các hydrocacbon mà chúng ta đang thảo luận là hydrocacbon mạch hở, bao gồm các một chuỗi các nguyên tử cacbon thẳng hàng. Đôi khi chúng cũng có thể tạo thành một vòng chỉ có các liên kết đơn như cyclopentan và cyclohexan.
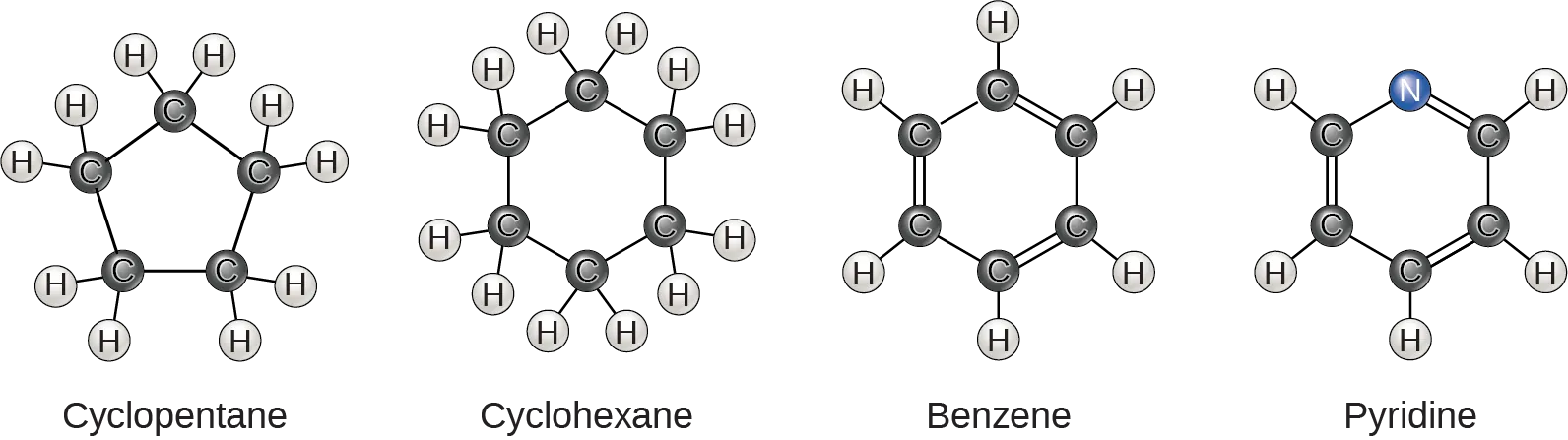
Một loại hydrocacbon khác – hydrocacbon thơm, bao gồm một vòng các nguyên tử cacbon với các liên kết đơn và đôi xen kẽ, chẳng hạn như benzen.
Đồng phân
Như vậy, việc xác định vị trí của các nguyên tử và liên kết hóa học trong không gian ba chiều của các phân tử hữu cơ là một yếu tố cốt lõi để hiểu được các đặc tính hóa học của chúng. Và chúng ta thường gọi những phân tử có cùng công thức hóa học nhưng khác nhau về mặt cấu trúc là đồng phân.
Các đồng phân cấu trúc, chẳng hạn như butan và isobutan, có sự khác nhau về vị trí của các liên kết cộng hóa trị: cả hai phân tử đều có bốn nguyên tử cacbon và mười nguyên tử hydro (C4H10), nhưng sự sắp xếp khác nhau của các nguyên tử trong phân tử đã dẫn đến sự khác biệt về tính chất hóa học của chúng. Ví dụ, butan thường được sử dụng làm nhiên liệu cho bật lửa và đèn khò, trong khi isobutan thường được sử dụng để chế tạo chất làm lạnh và chất đẩy trong bình xịt.
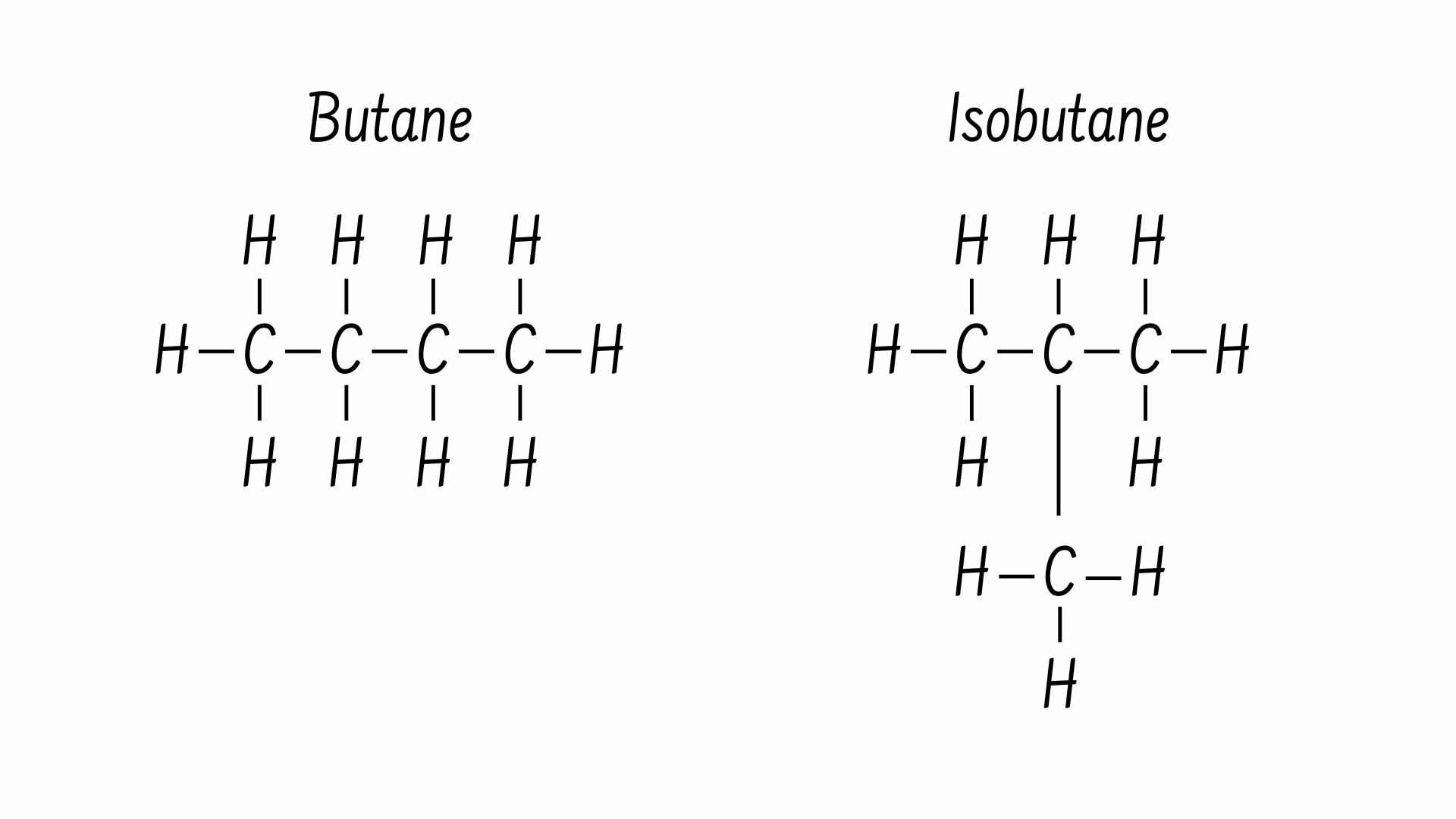
Đối với các đồng phân hình học, vị trí của liên kết cộng hóa trị là giống nhau nhưng các liên kết xung quanh nó lại khác nhau. Đối với buten (C4H8), hai nhóm metyl (CH3) có thể nằm ở cùng một phía hoặc ở hai phía của liên kết đôi ở trung tâm, lần lượt được gọi là cấu hình cis và cấu hình trans.
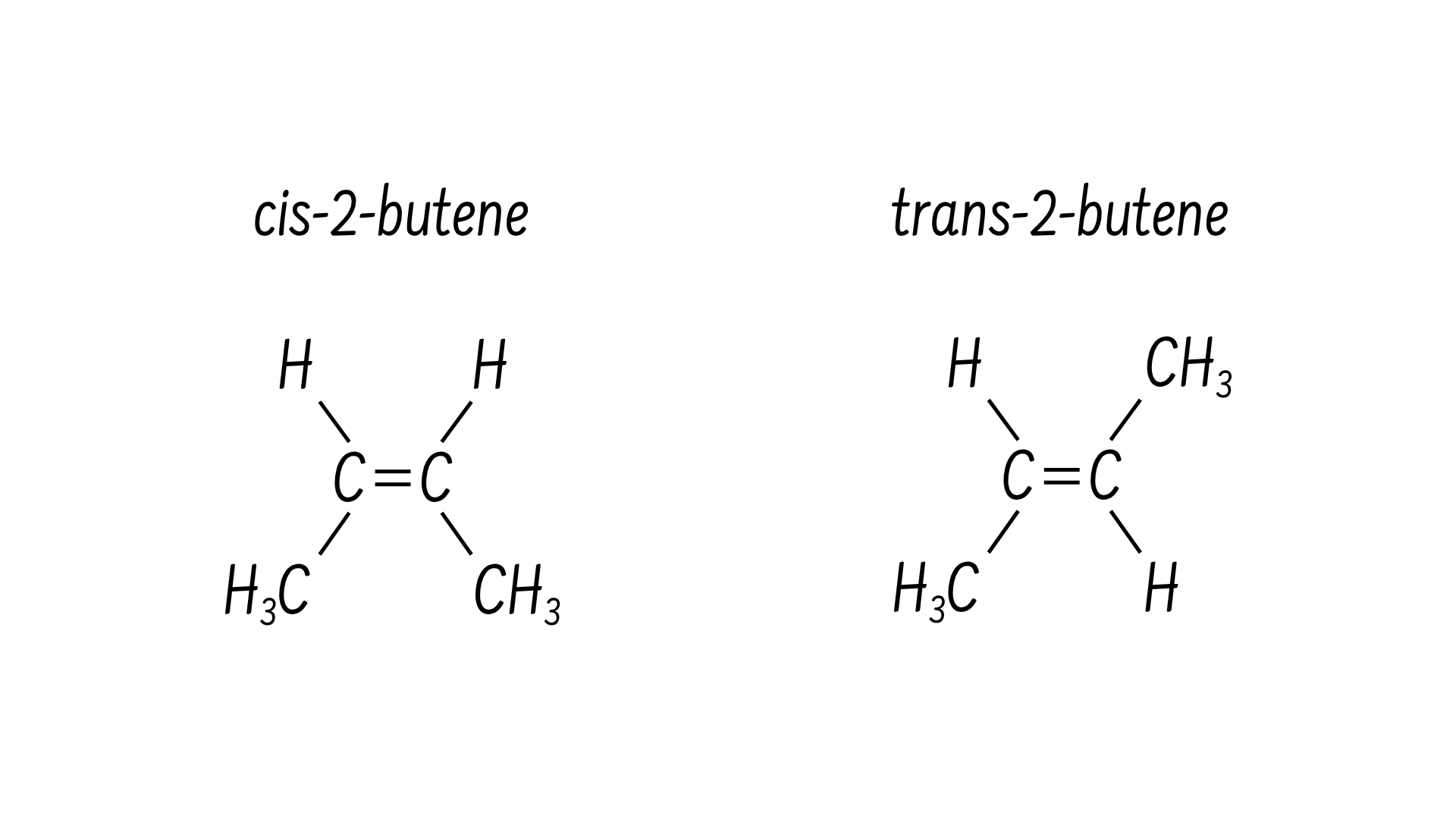
Trong triglyceride (chất béo và dầu), một chuỗi cacbon dài được gọi là axit béo có thể chứa các liên kết đôi, thường có hai cấu hình cis hoặc trans. Chất béo có ít nhất một liên kết đôi giữa các nguyên tử cacbon là chất béo không bão hòa. Ở cấu hình cis, việc khung carbon bị uốn cong về cùng một phía đã khiến các phân tử triglyceride không thể liên kết chặt chẽ với nhau, do đó chúng sẽ tồn tại ở dạng lỏng (dầu) ở nhiệt độ bình thường.
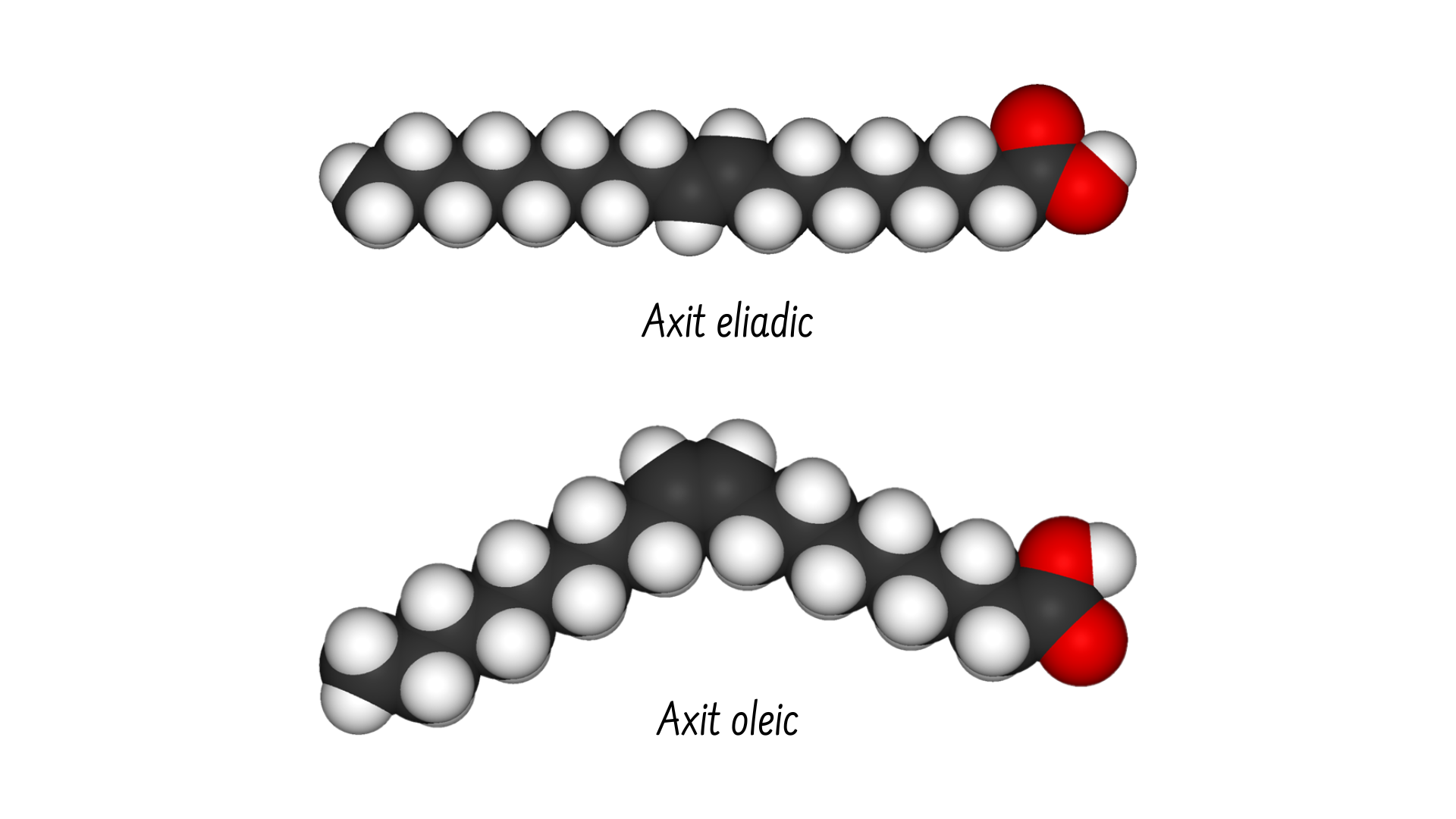
Ngược lại, triglyceride có liên kết đôi ở dạng cấu hình trans có các axit béo tương đối thẳng và có khả năng liên kết chặt chẽ với nhau, từ đó tạo thành chất béo rắn. Trong chế độ ăn của con người, chất béo trans có liên quan đến nguy cơ mắc các bệnh về tim mạch cao hơn, vì vậy lượng tiêu thụ chất béo này đã giảm dần trong những năm gần đây.
Trái ngược với chất béo không bão hòa, chúng ta gọi triglyceride không có liên kết đôi giữa các nguyên tử cacbon là chất béo bão hòa, thường có dạng rắn ở nhiệt độ bình thường và có nguồn gốc từ động vật.
Các đồng phân đối quang là những phân tử có cùng một cấu trúc và liên kết hóa học nhưng lại có sự khác nhau về vị trí của các nguyên tử, do đó hai cấu trúc này không thể chồng khít lên nhau. Hình ảnh bên dưới là một ví dụ về axit amin alanin, trong đó hai cấu trúc này không thể hoàn toàn trùng khớp với nhau.
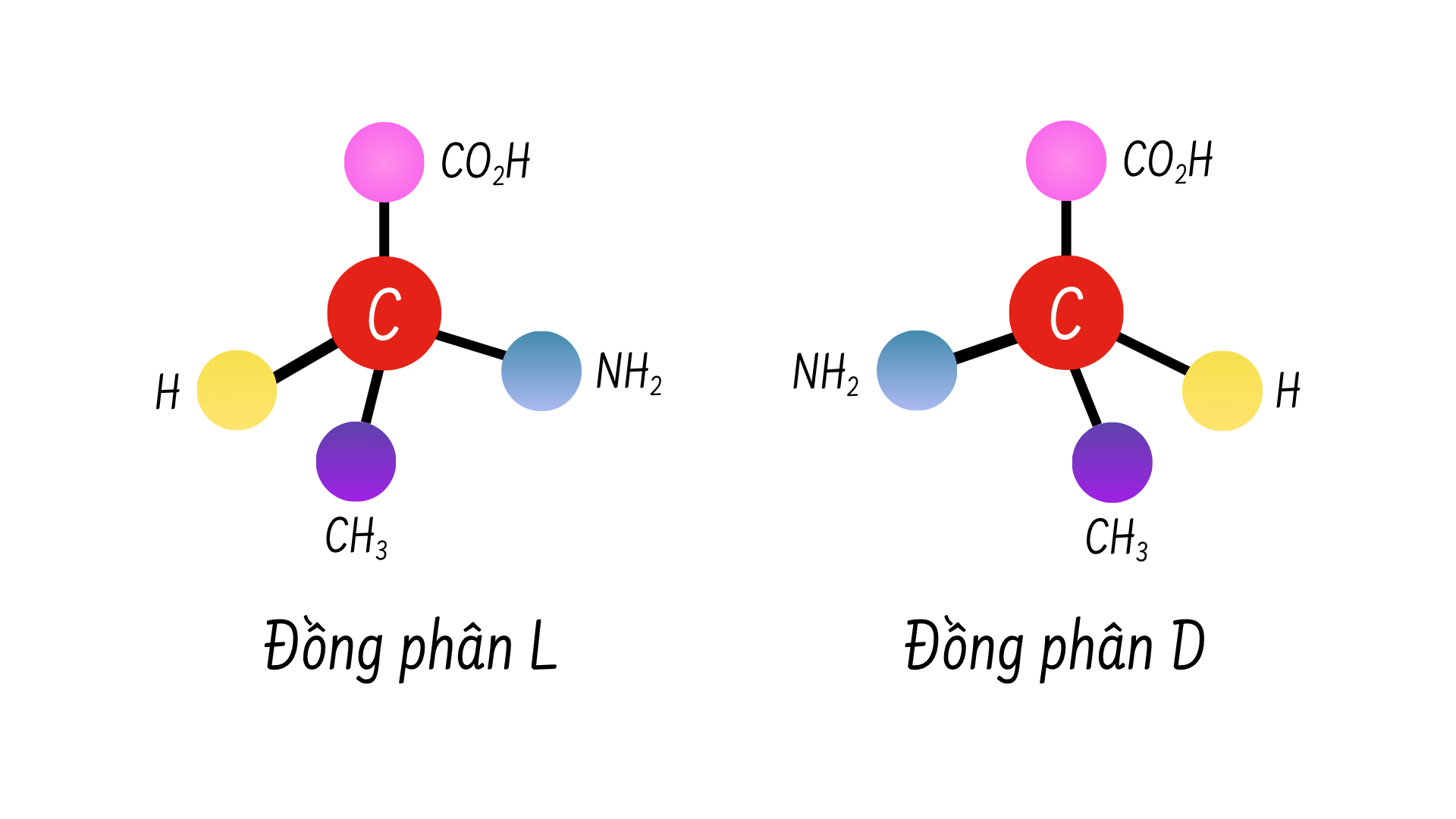
Nhóm chức
Nhóm chức là một nhóm các nguyên tử xuất hiện trong phân tử và tạo nên những tính chất hóa học đặc trưng cho các phân tử đó. Các nhóm chức này thường được gắn vào một hoặc nhiều vị trí khác nhau dọc theo “khung carbon” – đó có thể là một chuỗi hoặc một vòng các nguyên tử cacbon. Đôi khi, một nguyên tố cacbon trong bộ khung này có thể bị thay thế bởi một nguyên tố nitơ hoặc oxy, từ đó được gọi là hydrocarbon thế.
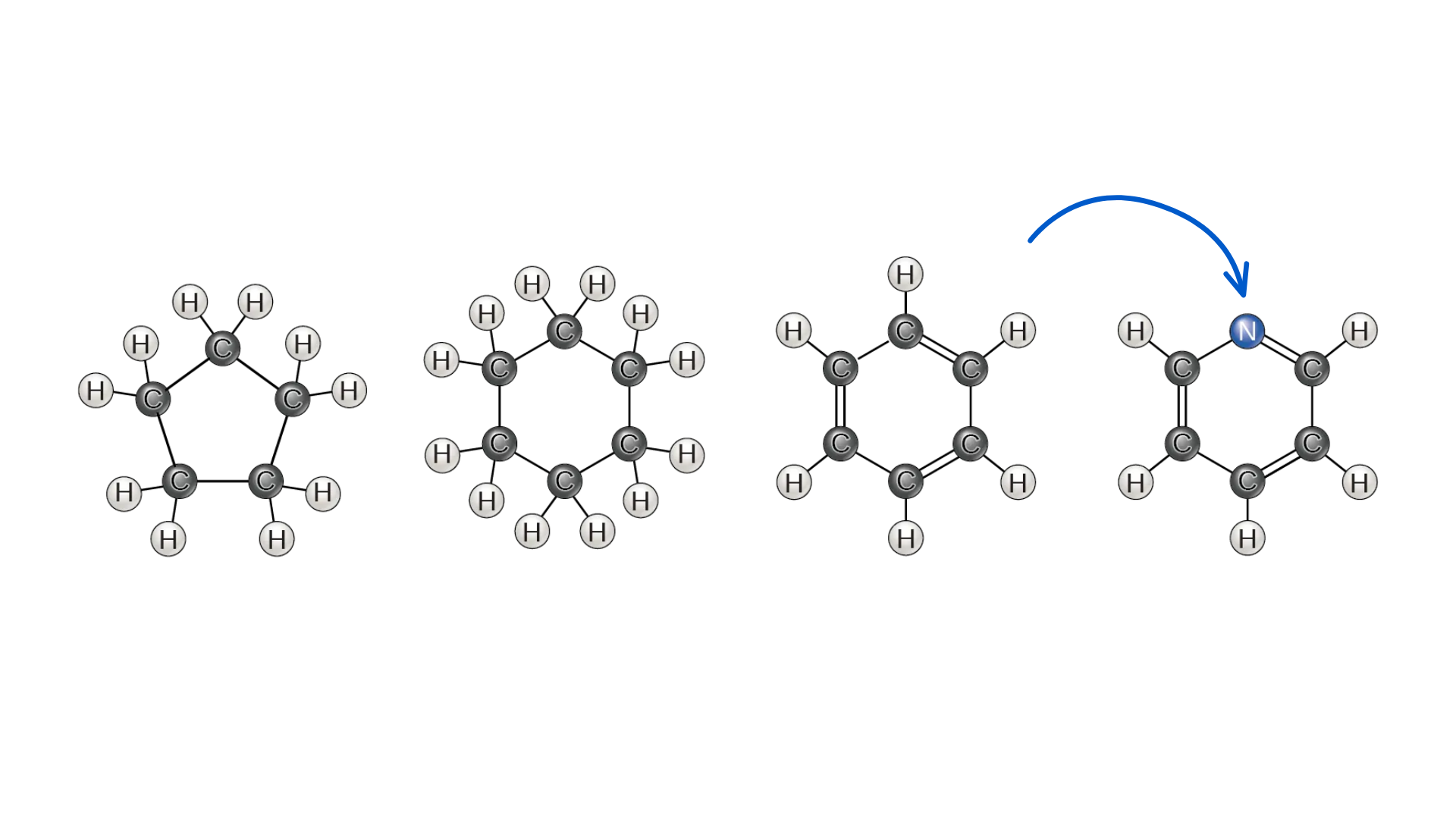
Bốn đại phân tử – protein, lipid, carbohydrate và axit nucleic – đều có một tập hợp các nhóm chức riêng, từ đó góp phần tạo nên các tính chất hóa học và chức năng khác nhau trong các sinh vật sống.
Nhóm chức có thể tham gia vào các phản ứng hóa học cụ thể. Các nhóm chức phổ biến nhất bao gồm: hydroxyl, methyl, carbonyl, carboxyl, amino, phosphate và sulfhydryl. Các nhóm này đóng vai trò quan trọng trong việc hình thành nên các phân tử như DNA, protein, carbohydrate và lipid.
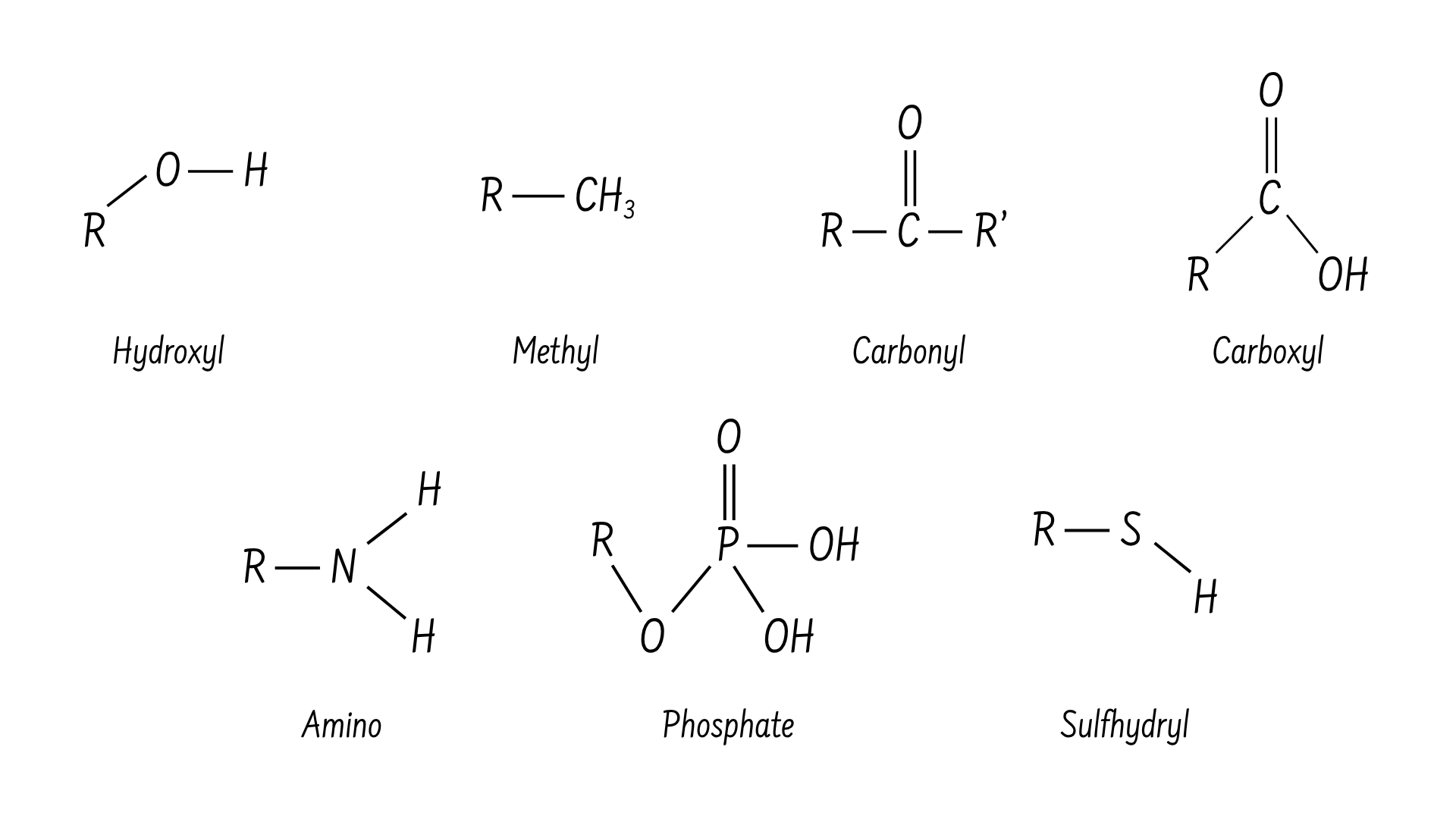
Chúng ta thường phân loại các nhóm chức là kỵ nước hoặc ưa nước tùy thuộc vào điện tích hoặc độ phân cực của chúng. Ví dụ về một nhóm chức kỵ nước chính là phân tử methyl không phân cực. Các nhóm chức ưa nước có thể kể đến là nhóm carboxyl. Nhóm này thường bị ion hóa để giải phóng các ion hydro (H+) từ nhóm COOH, tạo ra nhóm COO– mang điện tích âm và góp phần tạo nên tính chất ưa nước của bất kỳ phân tử nào chứa nhóm chức này. Các nhóm chức khác, chẳng hạn như nhóm carbonyl, có nguyên tử oxy mang điện tích âm một phần, có thể tạo nên liên kết hydro với các phân tử nước khác, làm cho phân tử chứa nhóm chức này trở nên ưa nước hơn.
Bên cạnh đó, liên kết hydro giữa các nhóm chức (trong cùng một phân tử hoặc giữa các phân tử khác nhau) đóng một vai trò rất quan trọng đối với chức năng của nhiều đại phân tử, giúp chúng gấp lại đúng cách và duy trì hình dạng thích hợp để có thể hoạt động một cách bình thường.
4. Các đại phân tử sinh học
Thức ăn cung cấp cho cơ thể các chất dinh dưỡng cần thiết để tồn tại. Nhiều chất dinh dưỡng thiết yếu này chính là các đại phân tử sinh học. Vậy thì những sinh vật sống cần những đại phân tử sinh học nào? Các phân tử này hình thành như thế nào? Chức năng của chúng là gì?
Tổng hợp các đại phân tử sinh học
Thường thì chúng ta có 4 đại phân tử sinh học chính (carbohydrate, lipid, protein và axit nucleic), tạo nên phần lớn “khối lượng khô” của tế bào (trong đó nước chiếm phần lớn khối lượng tổng thể của tế bào).
Hầu hết các đại phân tử đều được tạo nên từ các đơn vị riêng lẻ gọi là monomer. Các monome sẽ kết hợp với nhau bằng liên kết cộng hóa trị để tạo thành các phân tử lớn hơn được gọi là polymer. Trong quá trình này, các monome sẽ tạo ra nước đóng vai trò là một sản phẩm phụ và được gọi là phản ứng tổng hợp khử nước – một phản ứng liên kết các phân tử nhỏ hơn thành phân tử lớn hơn bằng cách “loại bỏ” các phân tử nước.
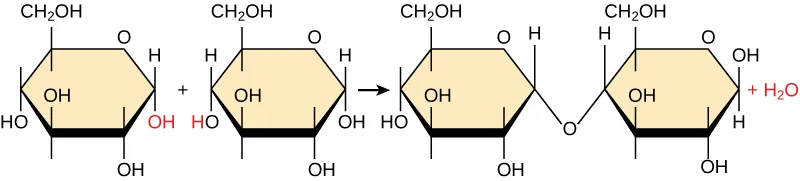
Trong phản ứng này, nguyên tử hydro của một monomer kết hợp với nhóm hydroxyl của một monomer khác và giải phóng một phân tử nước. Đồng thời, các monomer sẽ chia sẻ các electron và tạo thành các liên kết cộng hóa trị. Khi các monome khác tham gia, chuỗi các monomer này sẽ tạo thành một polymer.
Các loại monomer khác nhau có thể được kết hợp theo rất nhiều cách, tạo ra một nhóm các đại phân tử khác nhau. Ví dụ, các monomer glucose là thành phần có trong tinh bột, glycogen và cellulose.
Các polymer cũng có thể bị phân hủy thành các monomer trong quá trình thủy phân – một quá trình chèn một phân tử nước vào giữa các liên kết. Trong các phản ứng này, polymer sẽ bị phân tách thành hai phần: một phần nhận thêm một nguyên tử hydro (H+) và phần kia nhận thêm một phân tử hydroxyl (OH–) từ một phân tử nước bị tách ra.
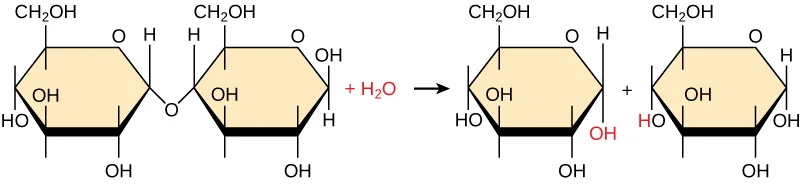
Và hai loại phản ứng này thường được xúc tác (hay “tăng tốc”) bởi các enzyme đặc hiệu. Phản ứng khử nước liên quan đến sự hình thành các liên kết mới và cần thu nhận năng lượng, trong khi phản ứng thủy phân sẽ phá vỡ các liên kết và giải phóng năng lượng.
Mỗi đại phân tử thường được phân giải bởi một hay nhiều enzyme cụ thể. Ví dụ, amylase, sucrase, lactase hoặc maltase sẽ phân giải carbohydrate. Các enzyme như protease (chẳng hạn như pepsin và peptidase) sẽ phân giải protein. Enzyme lipase thì sẽ phân giải lipid. Sau khi được phân giải, các đại phân tử sẽ cung cấp năng lượng cho các hoạt động của tế bào.
Carbohydrate
Hầu hết chúng ta ai cũng biết tới carbohydrate. Để giảm cân, một số người tuân theo chế độ ăn “ít carbohydrate”. Ngược lại, các vận động viên thường “nạp carbohydrate” để cung cấp đủ năng lượng giúp họ có thể thi đấu với phong độ cao nhất. Trong cuộc sống thường ngày, carbohydrate là một phần rất thiết yếu trong chế độ ăn uống của chúng ta. Ngũ cốc, trái cây và rau quả đều là nguồn carbohydrate tự nhiên cung cấp năng lượng cho cơ thể, đặc biệt là thông qua glucose, một loại đường đơn giản và là thành phần chính của tinh bột.
Công thức hóa học của carbohydrate là (CH2O)n – trong đó n là số nguyên tử cacbon có trong phân tử. Các nhà khoa học phân loại carbohydrate thành ba loại: monosaccharide, disaccharide và polysaccharide.
Monosaccharide (mono- = “một”; sacchar- = “ngọt”) là một loại đường đơn giản với ví dụ điển hình nhất là glucose. Trong monosaccharide, số lượng nguyên tử cacbon thường dao động từ 3 cho đến 7.
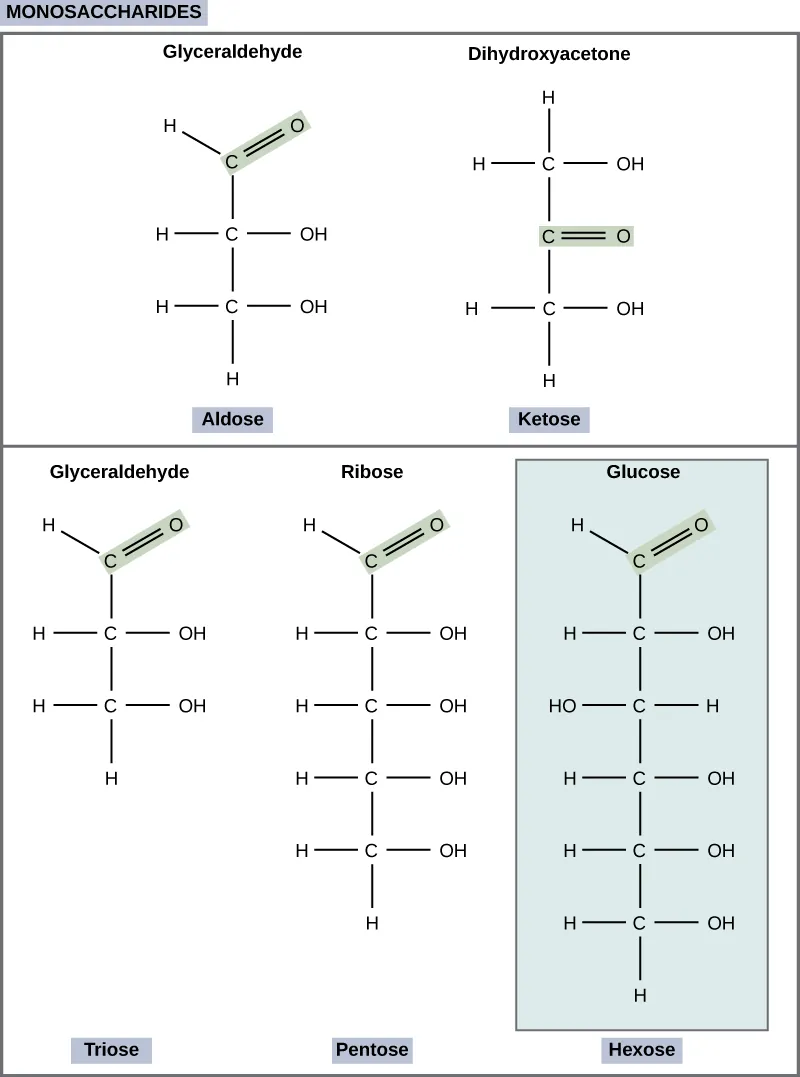
Hầu hết các monosaccharide đều kết thúc bằng hậu tố -ose. Nếu loại đường này có nhóm aldehyde (nhóm chức có cấu trúc R – CHO), nó sẽ là aldose. Và nếu nó có nhóm ketone (nhóm chức có cấu trúc RC(=O)R’), nó là ketose. Tùy thuộc vào số lượng nguyên tử cacbon có trong đường, chúng có thể là triose (ba nguyên tử cacbon), pentose (năm nguyên tử carbon) hoặc hexose (sáu nguyên tử carbon).
Ở người, glucose (C6H12O6)là một nguồn năng lượng rất quan trọng. Trong quá trình hô hấp tế bào, năng lượng được giải phóng từ glucose và giúp tạo ra adenosine triphosphate (ATP). Thực vật tổng hợp glucose bằng cách sử dụng cacbon dioxit và nước; glucose đến lượt nó cung cấp năng lượng cần thiết cho cây. Con người và các động vật khác ăn thực vật thường thu được glucose từ tinh bột được chuyển hóa.
Galactose (một phần của lactose, hay đường sữa) và fructose (có trong sucrose, hay trái cây) là những monosaccharide phổ biến khác. Mặc dù glucose, galactose và fructose đều có cùng công thức hóa học (C6H12O6) nhưng chúng lại có sự khác nhau về cấu trúc (đồng phân cấu trúc) do sự sắp xếp khác nhau của các nhóm chức xung quanh nguyên tử cacbon bất đối xứng.
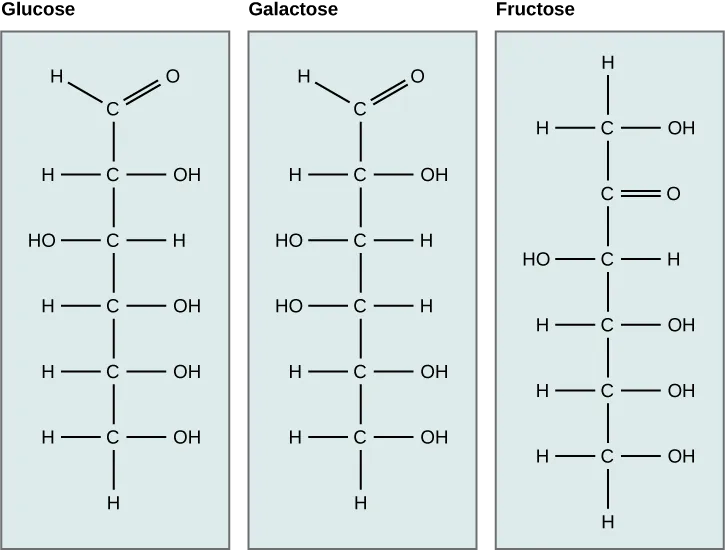
Các monosaccharide có thể tồn tại dưới dạng chuỗi thẳng hoặc dạng vòng. Trong nước, chúng thường xuất hiện dưới dạng vòng. Glucose ở dạng vòng có thể có hai cách sắp xếp nhóm hydroxyl (OH) xung quanh cacbon anomeric. Nếu nhóm hydroxyl nằm dưới cacbon anomeric trong đường, nó sẽ ở vị trí alpha (α). Và nếu nó nằm trên cacbon anomeric, nó ở vị trí beta (β)
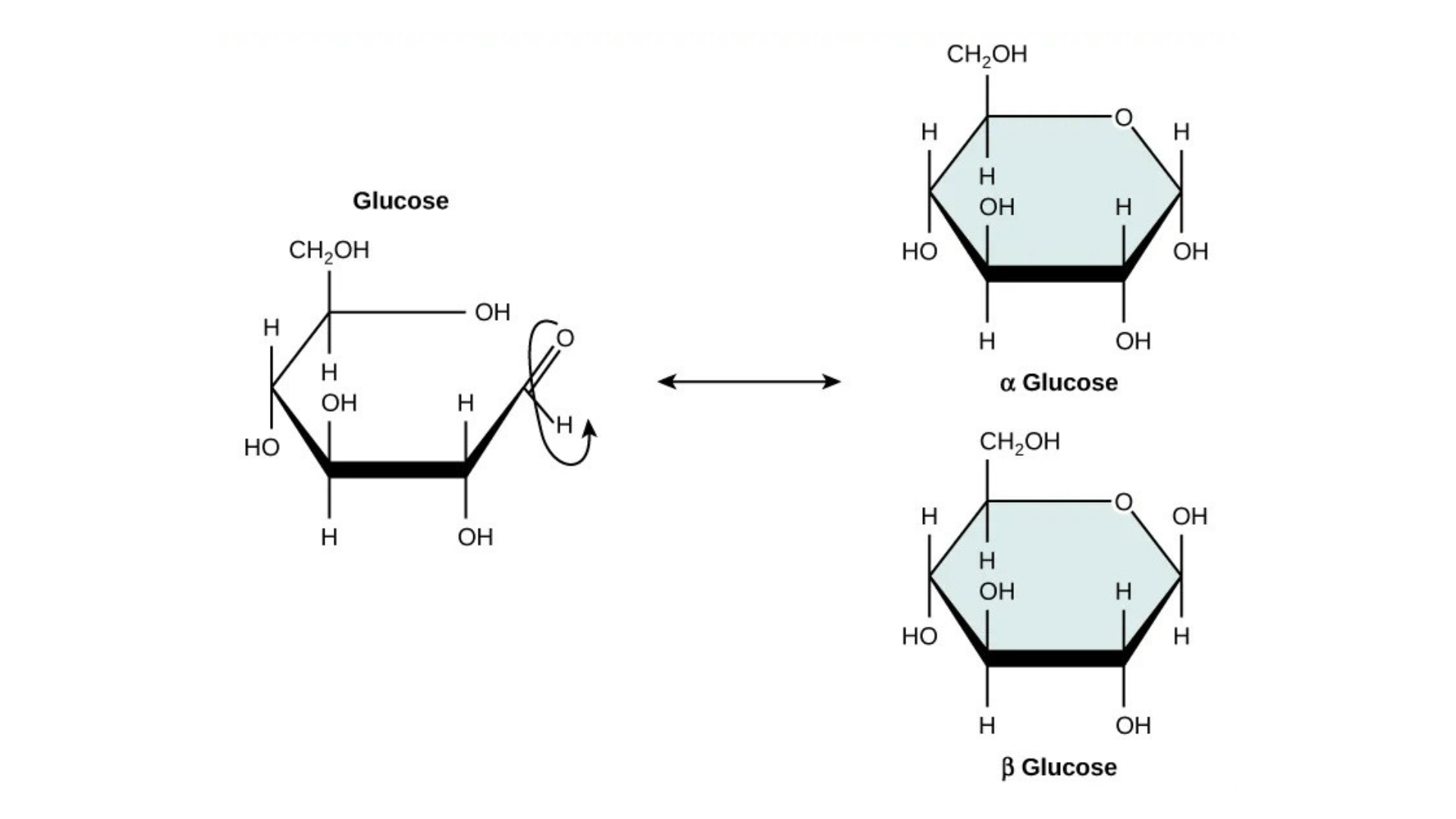
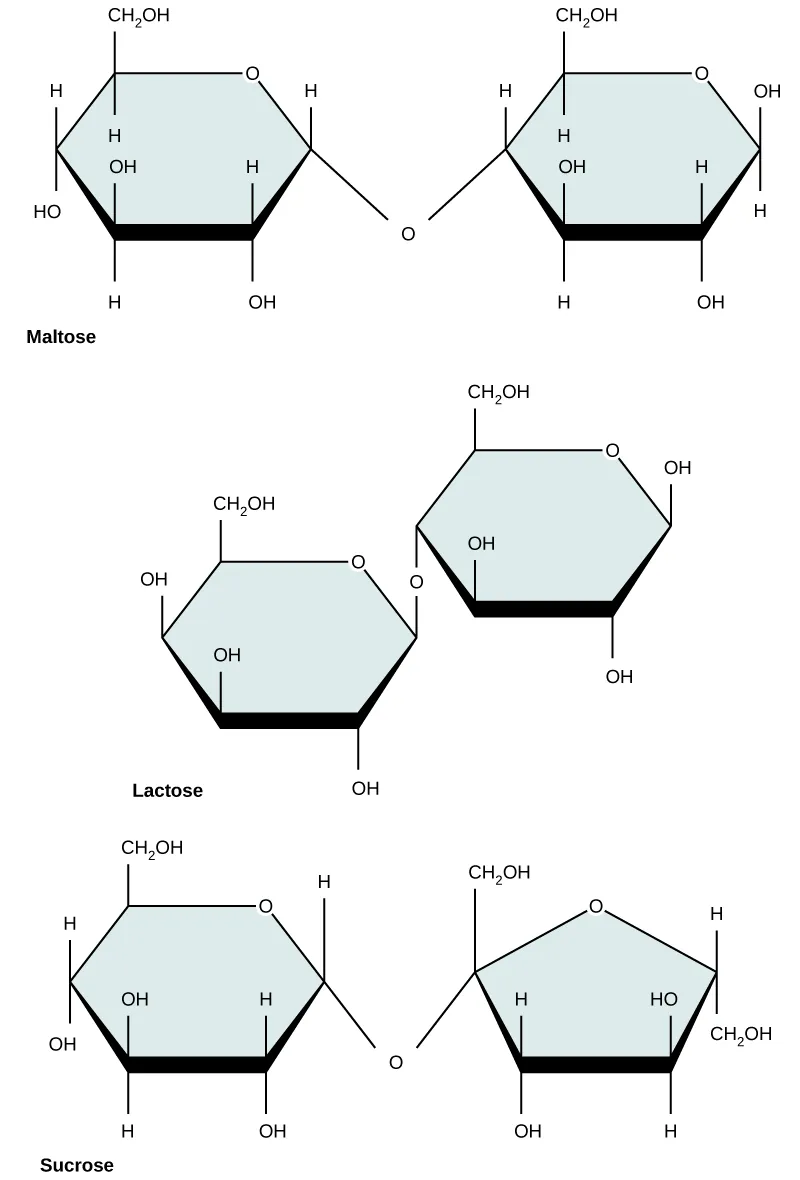
Disaccharide (di- = “hai”) được hình thành khi hai monosaccharide trải qua phản ứng tổng hợp khử nước. Trong quá trình này, nhóm hydroxyl của một monosaccharide kết hợp với hydro của monosaccharide khác, giải phóng một phân tử nước và tạo thành liên kết cộng hóa trị. Các nhà khoa học gọi đây là liên kết glycosidic.
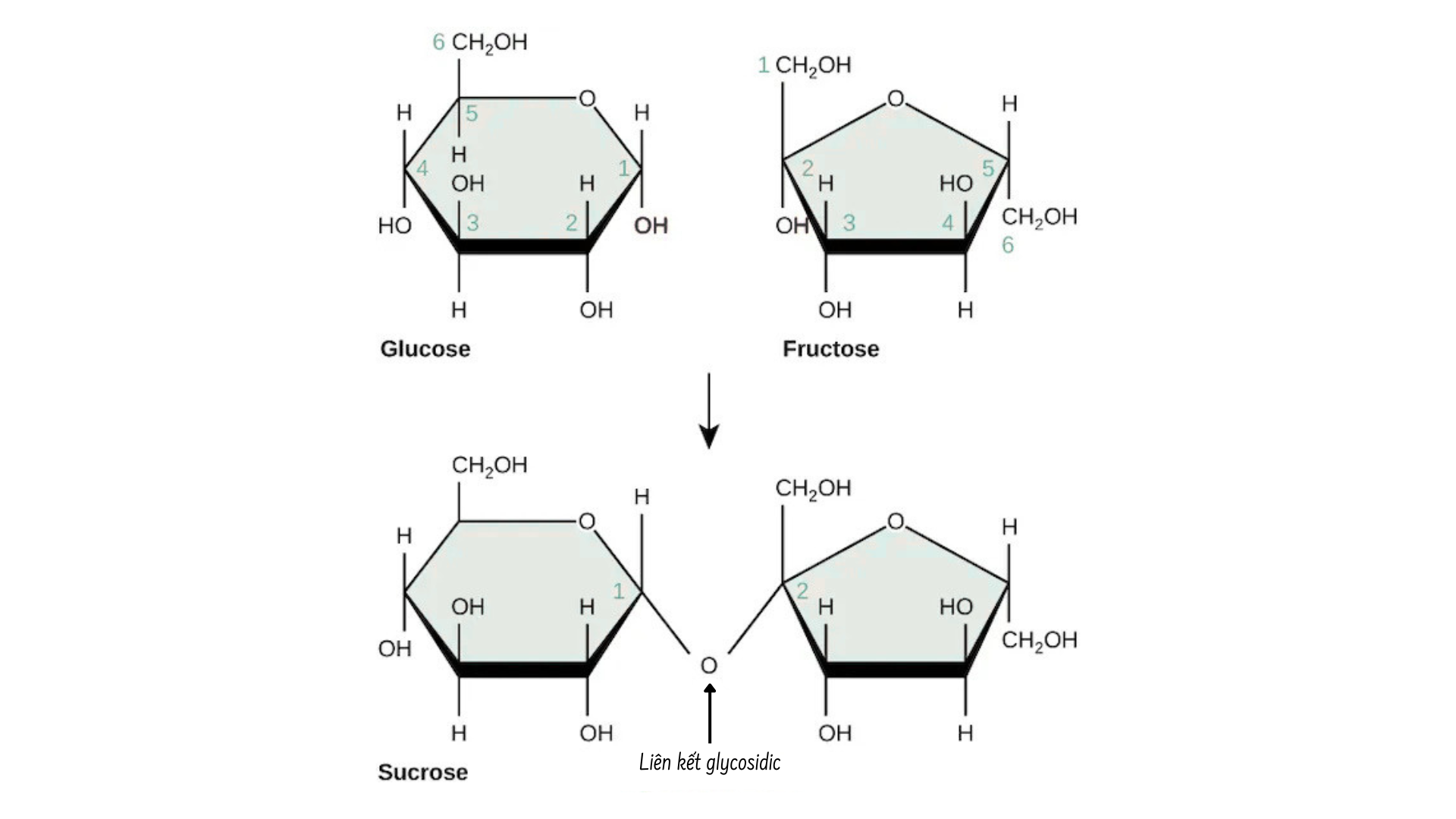
Liên kết glycosidic có thể là loại alpha hoặc beta. Liên kết alpha được hình thành khi nhóm OH của cacbon-1 nằm ở bên dưới và liên kết beta được hình thành khi nhóm OH của cacbon-1 nằm ở bên trên.
Các disaccharide phổ biến nhất bao gồm lactose, maltose và sucrose. Lactose là một disaccharide gồm các monome glucose và galactose. Nó xuất hiện rất nhiều ở trong sữa. Maltose, hay đường mạch nha, là một disaccharide được hình thành bởi phản ứng tổng hợp khử nước giữa hai phân tử glucose. Disaccharide phổ biến nhất là sucrose, hay đường ăn, bao gồm các monome glucose và fructose.
Polysaccharide (poly- = “nhiều”) là một chuỗi dài các monosaccharide liên kết với nhau bằng liên kết glycosidic. Chuỗi này có thể phân nhánh hoặc không phân nhánh và có thể chứa nhiều loại monosaccharide khác nhau. Tinh bột, glycogen, cellulose và chitin là những ví dụ điển hình nhất của polysaccharide.
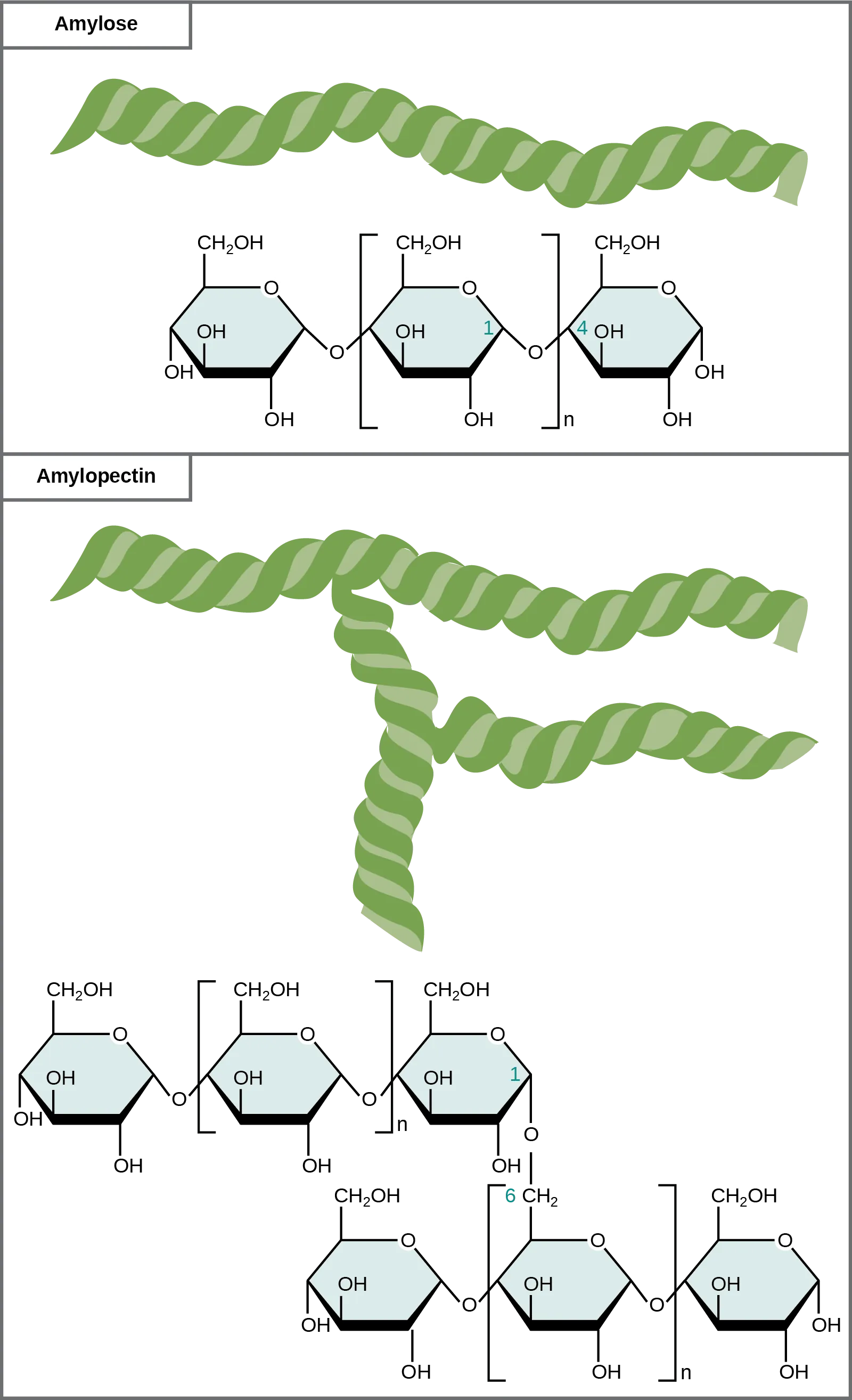
Thực vật dự trữ đường dưới dạng tinh bột. Trong thực vật, hỗn hợp amylose và amylopectin (cả hai đều là polymer glucose) tạo nên các loại đường này. Thực vật có khả năng tổng hợp glucose và chúng dự trữ lượng glucose dư thừa này trong các bộ phận khác nhau của cây, bao gồm rễ và hạt. Và các enzyme sẽ phân giải tinh bột. Ví dụ, amylase có trong nước bọt của chúng ta sẽ phân giải tinh bột này thành các phân tử nhỏ hơn, chẳng hạn như maltose và glucose. Sau đó, các tế bào có thể hấp thụ glucose.
Tinh bột glucose bao gồm các monome được liên kết với nhau bằng liên kết glycosidic α 1-4 hoặc α 1-6. Trong đó, liên kết α 1-4 sẽ là liên kết không phân nhánh còn liên kết α 1-6 sẽ là liên kết phân nhánh.
Glycogen là một dạng dự trữ glucose ở người và các loài động vật có xương sống khác, được cấu tạo từ các monome glucose và thường được lưu trữ trong tế bào gan và cơ. Khi lượng đường trong máu giảm, glycogen sẽ bị phân giải để giải phóng các glucose.
Cellulose là một polymer dồi dào nhất trong tự nhiên, chủ yếu làm nên thành tế bào thực vật. Gỗ và giấy chủ yếu là các sợi cellulose. Các monomer glucose cấu thành nên cellulose được liên kết với nhau bởi các liên kết glycosidic β 1-4
Cellulose có độ cứng và độ bền rất cao. Trong khi các enzyme tiêu hóa của con người không thể phân giải liên kết β 1-4, các động vật ăn cỏ như trâu hoặc bò, với sự trợ giúp của hệ vi khuẩn chuyên biệt trong dạ cỏ, có thể tiêu hóa được các loài thực vật giàu cellulose này nhờ vào enzyme có tên là cellulase. Cellulase có thể phân giải cellulose thành các monome glucose để cung cấp năng lượng. Mối cũng có khả năng phân giải cellulose nhờ sự hiện diện của các sinh vật khác bên trong cơ thể của chúng tiết ra cellulase.
Carbohydrate cũng xuất hiện rất phổ biến ở các loài động vật khác. Động vật chân đốt (côn trùng, giáp xác và các loài khác) có một bộ xương ngoài giúp bảo vệ các bộ phận bên trong cơ thể. Bộ xương này được làm nên từ chitin, một loại polysaccharide chứa nitơ. Chitin cũng là thành phần chính bên trong thành tế bào nấm.

Từ lâu, carbohydrate đã là một phần rất quan trọng trong chế độ ăn của con người trong hàng nghìn năm. Các loại thực phẩm phổ biến nhất có thể kể đến bao gồm lúa mì, gạo và ngô.
Bên cạnh đó, carbohydrate cũng bao gồm các thành phần hòa tan và không hòa tan. Phần không hòa tan, chất xơ, chủ yếu là cellulose. Chất xơ có rất nhiều công dụng. Nó thúc đẩy nhu động ruột đều đặn bằng cách tăng khối lượng phân và điều chỉnh tốc độ tiêu thụ glucose trong máu. Chất xơ cũng giúp loại bỏ cholesterol dư thừa ra khỏi cơ thể bằng cách liên kết với cholesterol trong ruột non, ngăn chặn các hạt cholesterol đi vào máu và được đào thải ra khỏi cơ thể thông qua phân. Chế độ ăn giàu chất xơ cũng giúp làm giảm nguy cơ mắc ung thư ruột kết.
Là một nguồn “năng lượng tức thời”, glucose bị phân hủy trong quá trình hô hấp tế bào và tạo ra ATP – một đơn vị năng lượng của tế bào. Nếu không tiêu thụ carbohydrate, lượng “năng lượng tức thời” có sẵn sẽ giảm xuống và gây ra cảm giác uể oải và mệt mỏi.
Lipid
Lipid là một nhóm các hydrocarbon có các liên kết carbon – carbon hoặc carbon – hydro không phân cực. Và các phân tử không phân cực thường có tính kỵ nước (sợ nước) hay không tan trong nước.
Các phân tử chất béo bao gồm hai thành phần chính – glycerol và axit béo. Glycerol là một hợp chất hữu cơ có 3 nguyên tử cacbon, 5 nguyên tử hydro và 3 nhóm hydroxyl (OH). Axit béo là một chuỗi hydrocarbon dài và một nhóm carboxyl (COOH) được gắn vào.
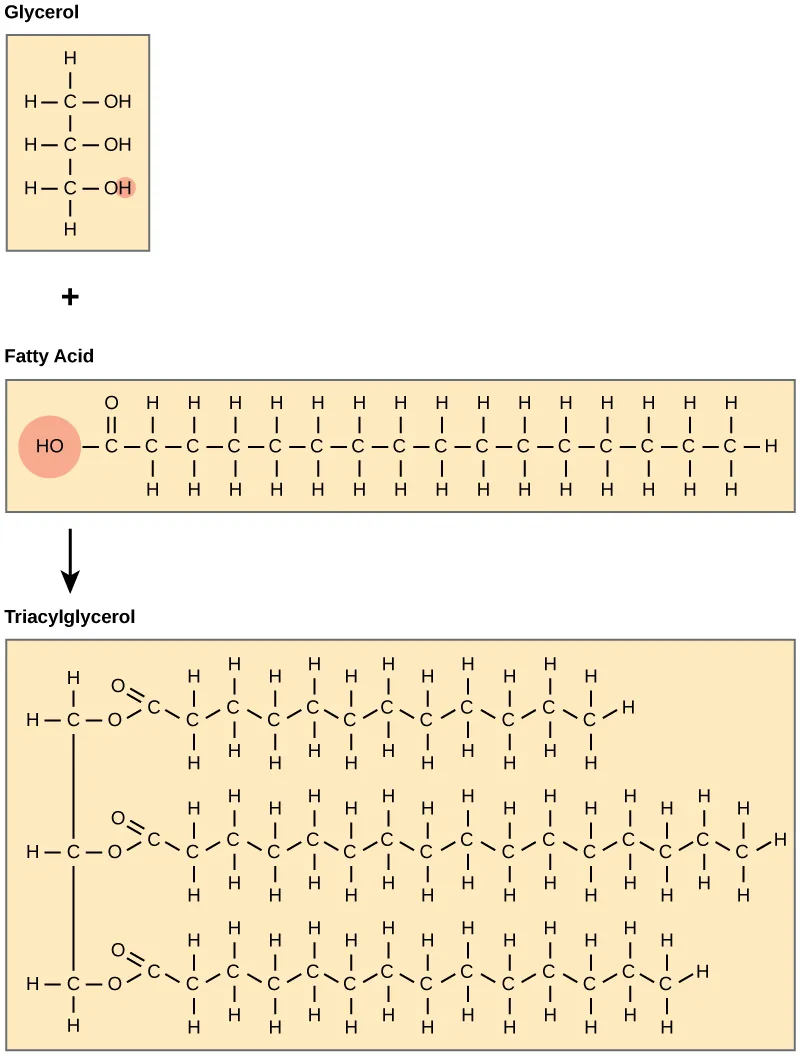
Số lượng cacbon trong axit béo có thể dao động từ 4 đến 36, phổ biến nhất là những axit béo chứa 12 đến 18 cacbon. Trong phân tử chất béo, các axit béo sẽ gắn vào ba nguyên tử cacbon của phân tử glycerol bằng liên kết este thông qua một nguyên tử oxy. Trong quá trình hình thành liên kết este này, ba phân tử nước sẽ được giải phóng.
Axit béo có thể là bão hòa hoặc không bão hòa. Trong một chuỗi axit béo, nếu các nguyên tử cacbon chỉ được liên kết với nhau bằng các liên kết đơn thì đây là một axit béo bão hòa – tức là số lượng nguyên tử hydro gắn vào khung cacbon đã đạt đến mức tối đa. Axit stearic là một ví dụ về axit béo bão hòa.
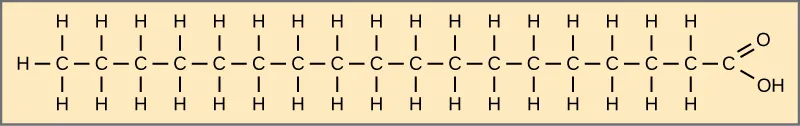
Mỡ động vật có axit stearic và axit palmitic (thường có trong thịt) và mỡ có axit butyric (thường có trong bơ) là những ví dụ khác về chất béo bão hòa (saturated fatty acid). Động vật có vú thường lưu trữ chất béo trong các tế bào chuyên biệt, hay tế bào mỡ, nơi các giọt chất béo chiếm phần lớn thể tích của tế bào.
Khi chuỗi hydrocarbon này chứa một liên kết đôi, axit béo này sẽ là axit béo không bão hòa. Axit oleic là một ví dụ về axit béo không bão hòa.
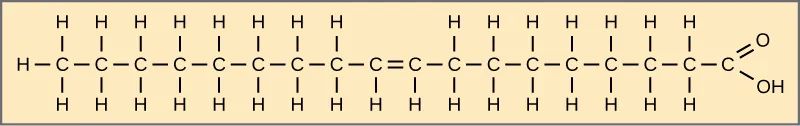
Hầu hết các chất béo không bão hòa (unsaturated fatty acid) đều ở dạng lỏng ở nhiệt độ phòng. Chúng ta gọi chúng là dầu. Nếu trong phân tử này có một liên kết đôi thì đó là chất béo không bão hòa đơn (ví dụ: dầu ô liu), và nếu có nhiều hơn một liên kết đôi thì đó là chất béo không bão hòa đa (ví dụ: dầu hạt cải)
Thực vật thường lưu trữ chất béo hoặc dầu trong hạt và sử dụng chúng làm nguồn năng lượng trong quá trình phát triển cây con. Chất béo, hoặc dầu không bão hòa thường có nguồn gốc thực vật và chứa các axit béo không bão hòa cis.
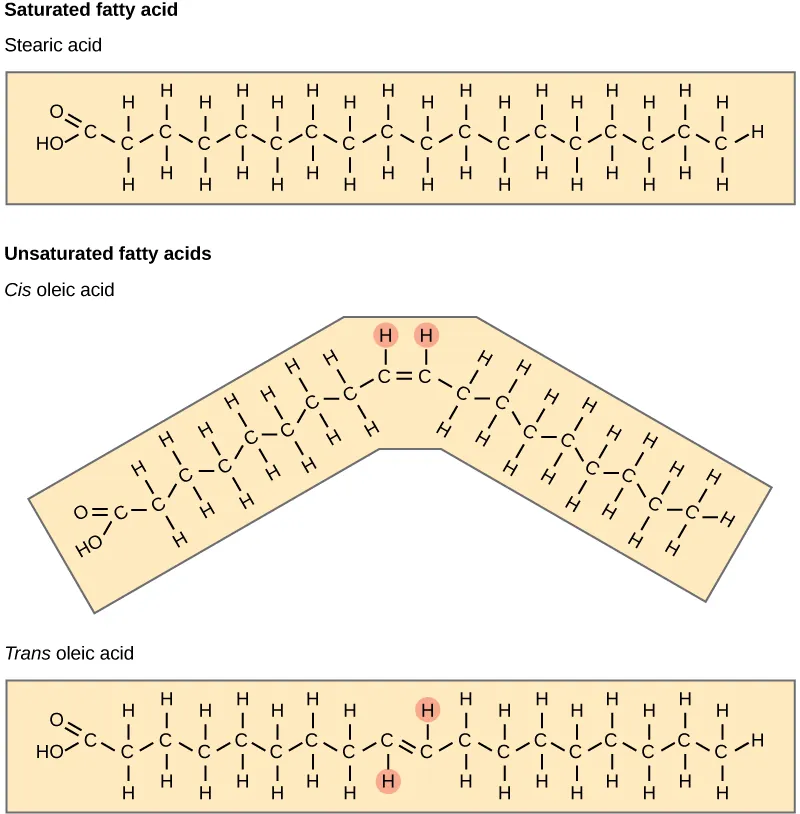
Như đã đề cập ở bên trên, cis và trans chỉ ra cấu hình của phân tử xung quanh liên kết đôi. Nếu các nguyên tử hydro nằm ở cùng một phía so với một mặt phẳng, đó là chất béo cis. Nếu các nguyên tử hydro nằm ở hai phía khác nhau so với một mặt phẳng, đó là chất béo trans. Liên kết đôi cis sẽ tạo ra một điểm bị “uốn cong” ngăn cản các axit béo liên kết chặt chẽ với nhau và giữ cho chúng ở dạng lỏng. Loại chất béo không bão hòa giúp làm giảm mức cholesterol trong máu. Trong khi đó, chất béo bão hòa lại góp phần hình thành nên mảng bám trong thành động mạch.
Ngày nay, ngành công nghiệp thực phẩm sử dụng phương pháp hydro hóa – một quá trình sục khí hydro vào dầu. Trong quá trình hydro hóa này, các liên kết đôi ở dạng cis trong chuỗi hydrocarbon có thể chuyển đổi thành các liên kết đôi ở dạng trans. Bơ thực vật và một số loại bơ đậu phộng là những ví dụ về chất béo chuyển hóa. Các nghiên cứu gần đây đã chỉ ra rằng việc tăng lượng chất béo chuyển hóa trong chế độ ăn có thể dẫn đến hàm lượng cholesterol “xấu” cao hơn, làm lắng đọng các mảng bám trong thành động mạch và gây ra các vấn đề về tim mạch.
Các axit béo thiết yếu là những axit béo mà cơ thể người cần nhưng không tự tổng hợp được. Do đó, chúng phải được bổ sung thông qua chế độ ăn uống. Axit béo omega-3 là một trong số các loại axit này, cùng với axit béo omega-6. Đây là các axit béo không bão hòa đa.
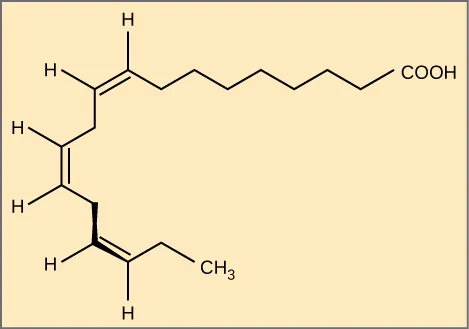
Giống như carbohydrate, chất béo cũng nhận được khá nhiều những lời chỉ trích và lên án. Đúng là ăn quá nhiều đồ chiên rán và các loại thực phẩm “nhiều chất béo” khác sẽ gây ra rất nhiều các vấn đề về sức khỏe. Tuy nhiên, chất béo cũng có những chức năng quan trọng. Có rất nhiều vitamin tan trong chất béo và chúng cũng là một dạng dự trữ năng lượng dài hạn của tế bào. Chúng cũng giúp cách nhiệt cho cơ thể. Do đó, chúng ta nên tiêu thụ chất béo “lành mạnh” với lượng vừa phải.
Sáp là một dạng chất béo khác bao phủ bộ lông của các loài chim thủy sinh và xuất hiện trên bề mặt lá ở một số loài thực vật. Do tính chất kỵ nước của sáp, chúng ngăn nước bám dính trên bề mặt.
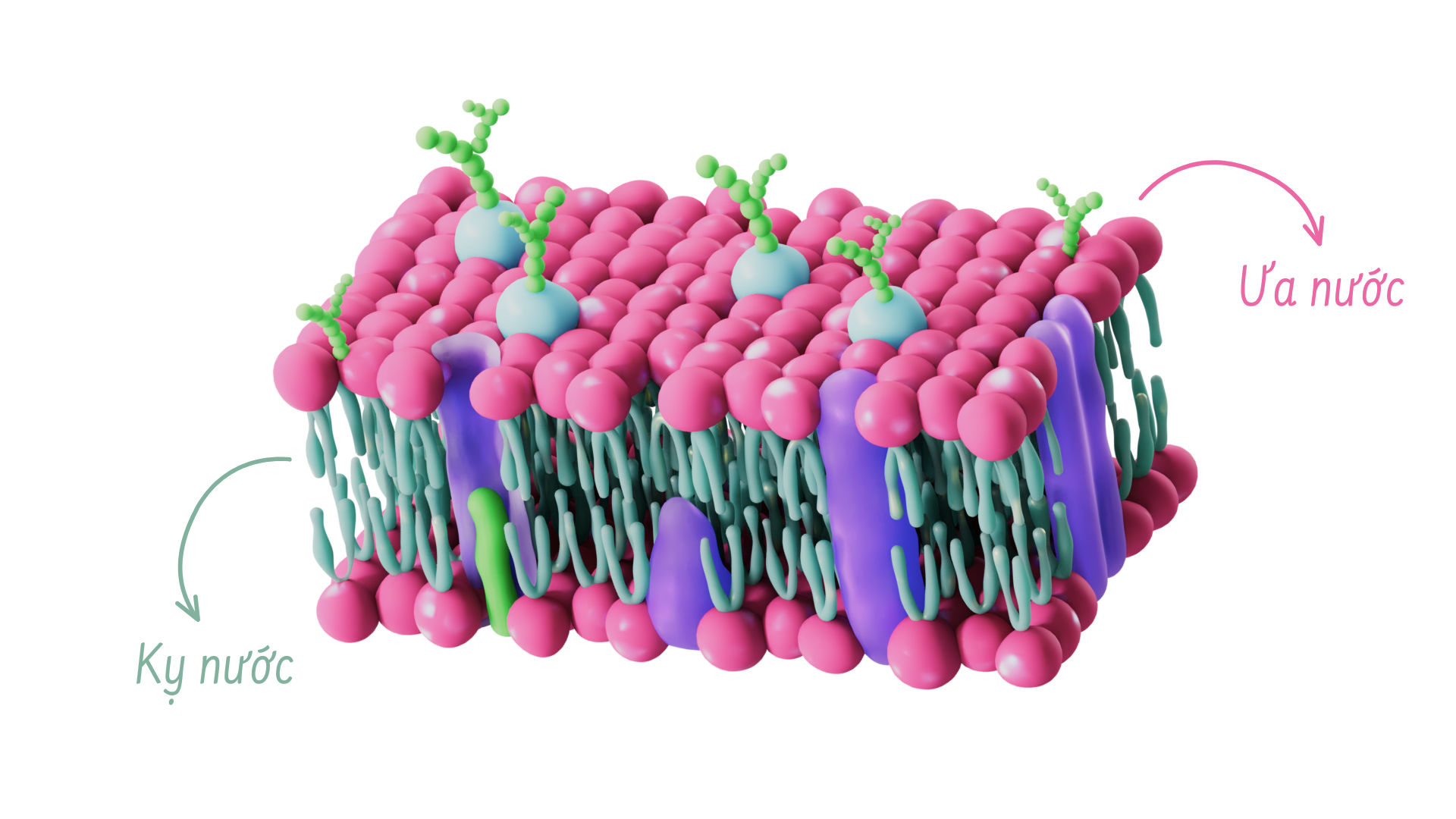
Phospholipid là thành phần chính làm nên màng tế bào. Giống như chất béo, chúng được cấu tạo từ các chuỗi axit béo gắn vào khung glycerol hoặc sphingosine. Tuy nhiên, thay vì có ba axit béo như trong triglyceride, phospholipid là một phân tử gồm hai axit béo và một nhóm phosphate biến tính gắn vào khung glycerol.
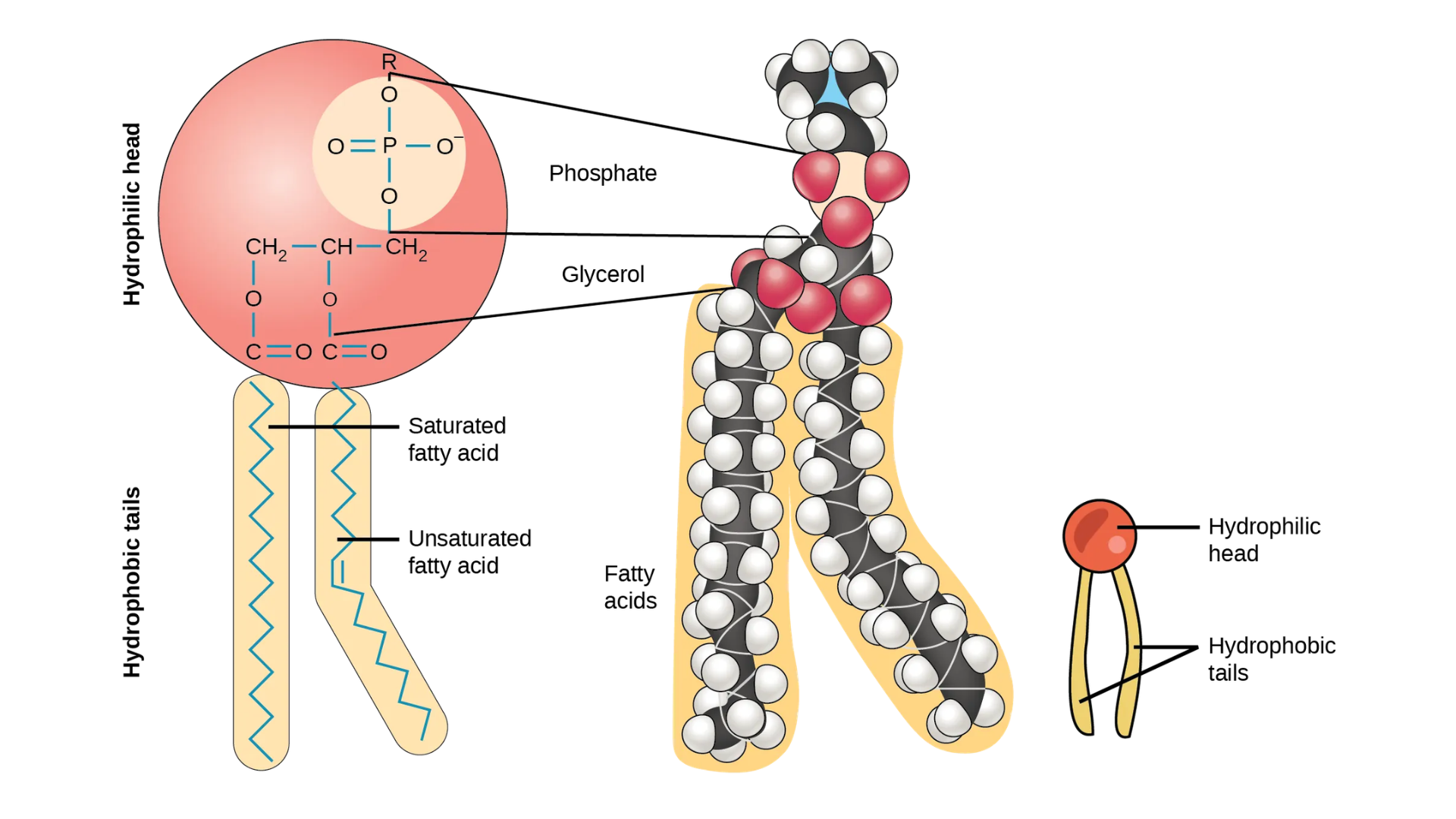
Phospholipid là một phân tử lưỡng cực, nghĩa là nó có một đầu kỵ nước và một đầu ưa nước. Các chuỗi axit béo là đầu kỵ nước và không thể tương tác với nước; trong khi nhóm chứa phosphate là đầu ưa nước và tương tác với nước.
Trong màng tế bào, lớp kép phospholipid với đuôi axit béo của phospholipid sẽ hướng vào bên trong và tránh xa nước. Trong khi đó, nhóm phosphate sẽ hướng ra bên ngoài và tiếp xúc với nước.
Không giống như phospholipid và chất béo, steroid có cấu trúc vòng khép kín. Mặc dù chúng không giống với các lipid khác nhưng các nhà khoa học vẫn xếp chúng vào nhóm này vì chúng cũng không tan trong nước. Tất cả các steroid đều có bốn vòng cacbon liên kết với nhau.
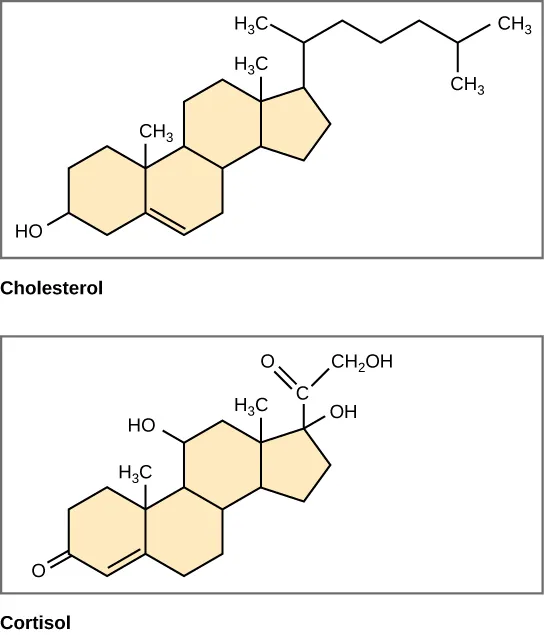
Cholesterol là loại steroid phổ biến nhất. Gan tổng hợp cholesterol và là tiền chất của nhiều hormone steroid như testosterone và estradiol, được tiết ra từ tuyến sinh dục và tuyến nội tiết. Nó cũng là tiền chất của vitamin D. Mặc dù cholesterol thường bị chỉ trích rất nhiều nhưng nó lại rất cần thiết cho các hoạt động bình thường của cơ thể.
Protein
Protein là một trong những phân tử hữu cơ dồi dào nhất trong các sinh vật sống và có rất nhiều loại khác nhau.
Đầu tiên chính là các enzyme – một chất xúc tác giúp tăng tốc các phản ứng hóa học bên trong các sinh vật sống. Có rất nhiều loại enzyme khác nhau và mỗi enzyme đều được “thiết kế riêng” để “phù hợp” với một số phân tử nhất định – được gọi là tính đặc hiệu đối với các chất nền. Chúng ta thường gọi các enzyme phân giải chất nền là enzyme dị hóa; những enzyme xây dựng các phân tử phức tạp hơn từ chất nền của chúng là enzyme đồng hóa và các enzyme ảnh hưởng đến tốc độ phản ứng là enzyme xúc tác. Một ví dụ về các enzyme là amylase trong nước bọt giúp thủy phân chất nền amylose, một thành phần của tinh bột.
Thứ hai, hormone là các phân tử tín hiệu được sản xuất bởi các tế bào nội tiết, có chức năng kiểm soát hoặc điều chỉnh các quá trình sinh học, bao gồm tăng trưởng, phát triển, trao đổi chất và sinh sản. Ví dụ, insulin là một hormone protein giúp điều chỉnh chỉ số đường huyết trong máu.
Sau đây là một số loại protein khác cùng với các chức năng đi kèm với chúng
| Phân loại | Ví dụ | Chức năng |
| Enzyme tiêu hoá | Amylase, lipase, pepsin, trypsin | Hỗ trợ quá trình tiêu hóa bằng cách phân giải chất dinh dưỡng thành các monomers. |
| Vận chuyển | Hemoglobin, albumin | Vận chuyển các chất trong máu hoặc bạch huyết đi khắp cơ thể. |
| Cấu trúc | Actin, tubulin, keratin | Xây dựng khung tế bào. |
| Hormones | Insulin, thyroxine | Điều phối hoạt động của cơ thể. |
| Phòng thủ | Immunoglobulins | Bảo vệ cơ thể khỏi các tác nhân gây bệnh. |
| Co thắt | Actin, myosin | Co cơ |
| Dự trữ | Protein dự trữ trong các loại đậu, lòng trắng trứng (albumin) | Cung cấp dưỡng chất trong giai đoạn phát triển phôi sớm và cây con. |
Tất cả các loại protein đều được cấu tạo từ 20 loại axit amin khác nhau – là các monomer cấu tạo nên protein. Về cơ bản, mỗi loại axit amin đều có cấu trúc giống nhau, bao gồm một nguyên tử carbon ở trung tâm (carbon alpha – α) liên kết với một nhóm amino (NH2), một nhóm carboxyl (COOH) và một nguyên tử hydro. Mỗi axit amin cũng có một nguyên tử hoặc nhóm nguyên tử khác liên kết với nguyên tử ở trung tâm được gọi là nhóm R (chuỗi bên)
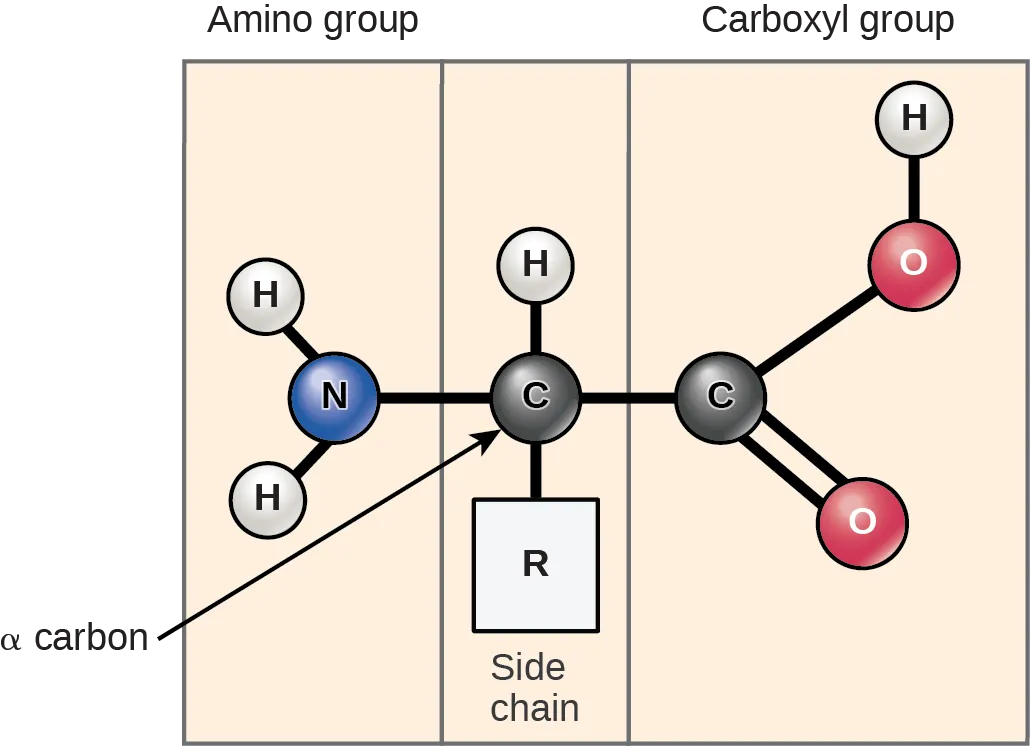
Trong số 20 loại axit amin phổ biến nhất, 9 trong số đó là các axit amin thiết yếu ở người vì cơ thể người không thể tự sản xuất ra chúng và phải thu nhận từ các loại thực phẩm ở bên ngoài.
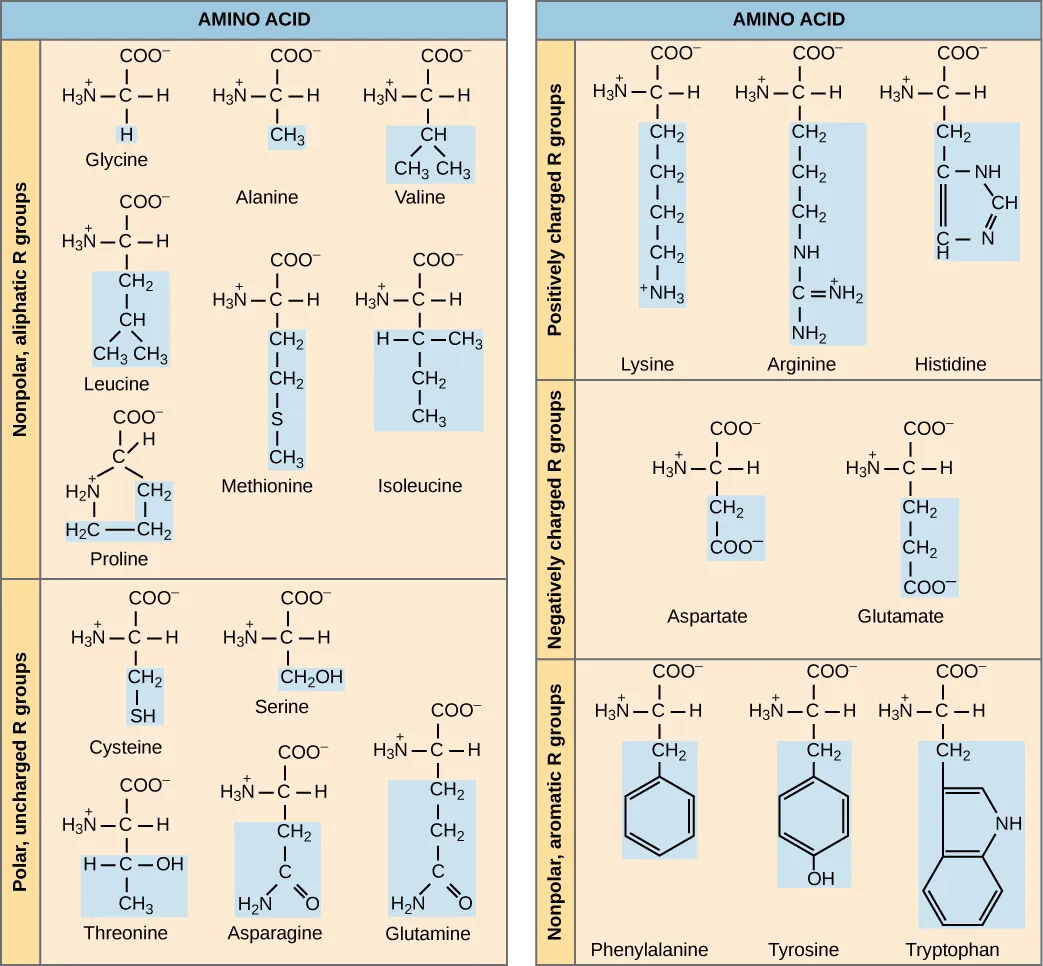
Đối với mỗi axit amin, nhóm R (chuỗi bên) sẽ là khác nhau. Và tính chất hóa học của chuỗi bên sẽ quyết định toàn bộ tính chất hoá học của axit amin (tính axit, bazơ, phân cực hay không phân cực). Ví dụ, glycine có một nguyên tử hydro làm nhóm R. Các axit amin như valine, methionine và alanine thì lại không phân cực (kỵ nước), trong khi các axit amin như serine, threonine và cysteine lại có tính phân cực (ưa nước). Chuỗi bên của lysine và arginine mang điện tích dương, do đó các axit amin này lại có tính bazơ. Proline có một nhóm R liên kết với nhóm amino, tạo thành cấu trúc dạng vòng.
Nhìn chung thì các loại axit amin thiết yếu ở người bao gồm isoleucine, leucine và cysteine (Axit amin thiết yếu là những axit amin cần thiết để xây dựng nên các protein bên trong cơ thể nhưng cơ thể không có khả năng tự sản xuất. Loại axit amin nào là thiết yếu sẽ tùy thuộc vào từng loài sinh vật)
Trình tự và số lượng axit amin sẽ quyết định hình dạng, kích thước và chức năng của protein. Một liên kết cộng hóa trị, hay liên kết peptide, được hình thành thông qua phản ứng tổng hợp khử nước: Nhóm carboxyl của một axit amin và nhóm amino của axit amin tiếp theo sẽ kết hợp với nhau và giải phóng một phân tử nước.
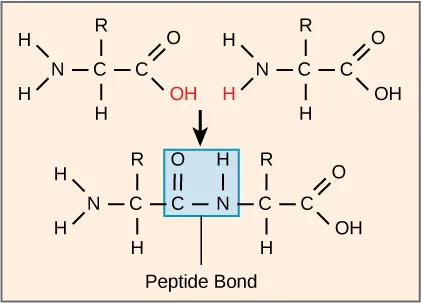
Khi càng có nhiều axit amin tham gia, chuỗi thu được là một polypeptide. Mỗi polypeptide có một nhóm amino tự do ở một đầu. Mặc dù thuật ngữ polypeptide và protein đôi khi được sử dụng thay thế cho nhau, nhưng polypeptide là một polymer của các axit amin, trong khi protein được sử dụng cho một hoặc nhiều polypeptide đã được kết hợp với nhau, có hình dạng riêng biệt và các chức năng độc đáo.
Protein có rất nhiều hình dạng và kích thước khác nhau. Ví dụ, hemoglobin là một protein hình cầu, nhưng collagen trong da của chúng ta lại là một protein dạng sợi. Và hình dạng của protein sẽ quyết định chức năng của nó. Nhưng để có thể hiểu được các hình dạng này của protein, chúng ta cần phải hiểu bốn cấp độ cấu trúc của nó: bậc 1, bậc 2, bậc 3 và bậc 4.
Trình tự độc đáo của các axit amin trong chuỗi polypeptide tạo nên cấu trúc bậc 1 của nó. Ví dụ, hormone insulin của tuyến tụy có hai chuỗi polypeptide, A và B, và chúng được liên kết với nhau bằng liên kết disulfide.
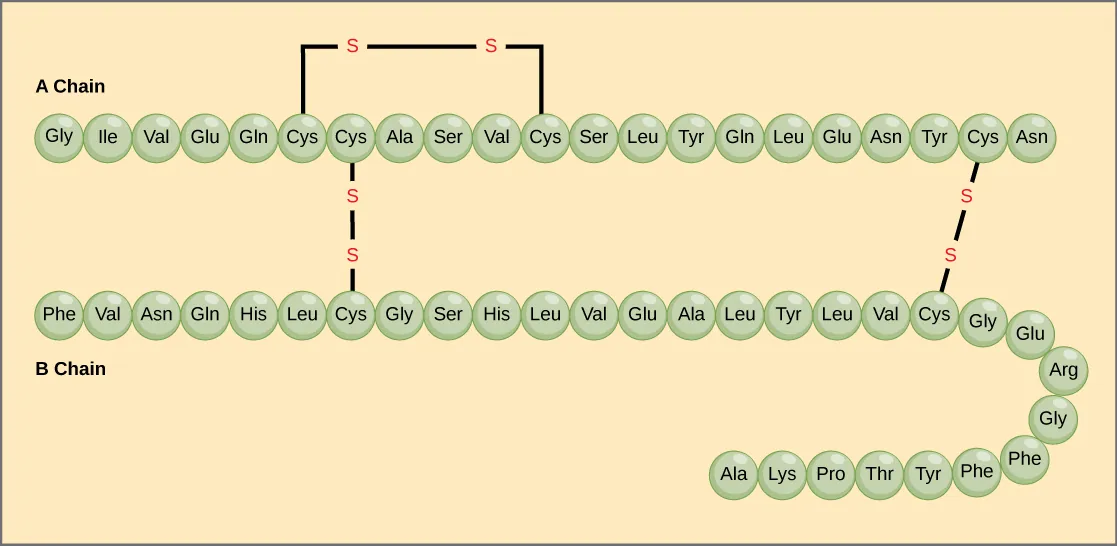
Các gen mã hóa protein sẽ quyết định trình tự duy nhất cho mỗi protein. Sự thay đổi trong trình tự nucleotide của vùng mã hóa gen có thể dẫn đến việc thêm một axit amin khác vào chuỗi polypeptide đang phát triển, gây ra sự thay đổi về mặt cấu trúc và chức năng của protein. Ví dụ, trong bệnh thiếu máu hồng cầu hình liềm, valine trong chuỗi β thế chỗ glutamic. Điều đặc biệt là một phân tử hemoglobin bao gồm hai chuỗi alpha và hai chuỗi beta, mỗi chuỗi có khoảng 150 axit amin. Do đó, phân tử này có khoảng 600 axit amin. Và sự khác biệt về mặt cấu trúc giữa một phân tử hemoglobin bình thường và một phân tử hemoglobin của bệnh thiếu máu hồng cầu hình liềm – làm giảm đáng kể tuổi thọ của người bệnh – chỉ là một axit amin duy nhất.
Lúc này, các phân tử hemoglobin sẽ tạo thành các sợi dài làm biến dạng các tế bào hồng cầu thành hình lưỡi liềm, từ đó làm tắc nghẽn mạch máu, dẫn đến khó thở, chóng mặt, đau đầu và đau bụng.
Tiếp theo, sự gấp khúc cục bộ của chuỗi polypeptide sẽ tạo ra cấu trúc bậc hai của protein, phổ biến nhất là cấu trúc xoắn α và cấu trúc tấm gấp β. Cả hai cấu trúc đều được hỗ trợ bởi liên kết hydro.
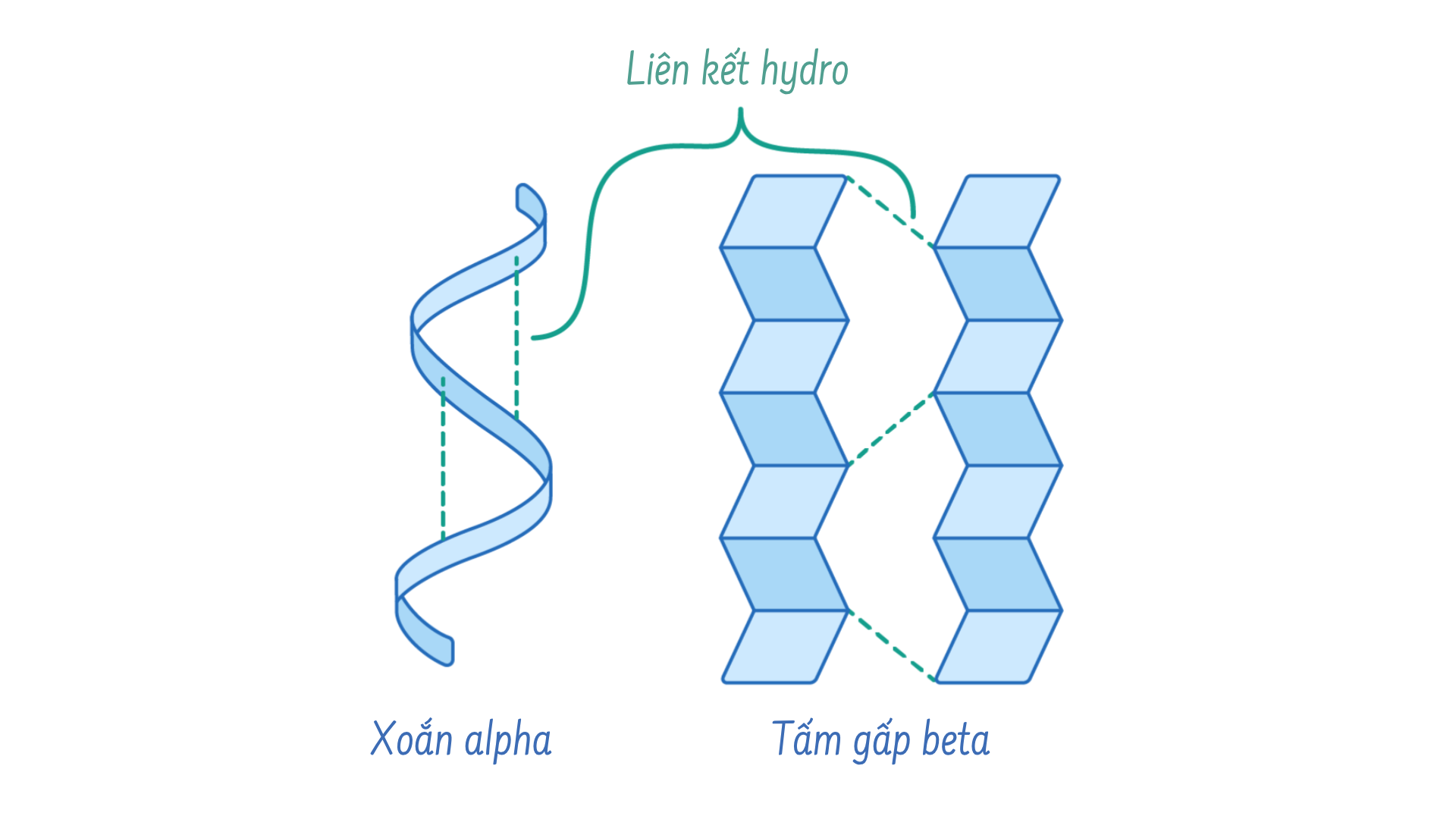
Cấu trúc ba chiều độc đáo của chuỗi polypeptide chính là cấu trúc bậc ba của nó. Chủ yếu thì các liên kết giữa các nhóm R sẽ tạo nên cấu trúc bậc ba phức tạp của protein. Ví dụ, các nhóm R mang điện tích cùng dấu sẽ đẩy nhau và các nhóm R mang điện tích trái dấu sẽ hút nhau. Khi quá trình “gấp” protein diễn ra, các nhóm R kỵ nước sẽ nằm bên trong protein; trong khi các nhóm R ưa nước sẽ nằm ở bên ngoài. Tất cả các tương tác này, dù mạnh hay yếu, đều sẽ quyết định tới hình dạng ba chiều cuối cùng của protein.
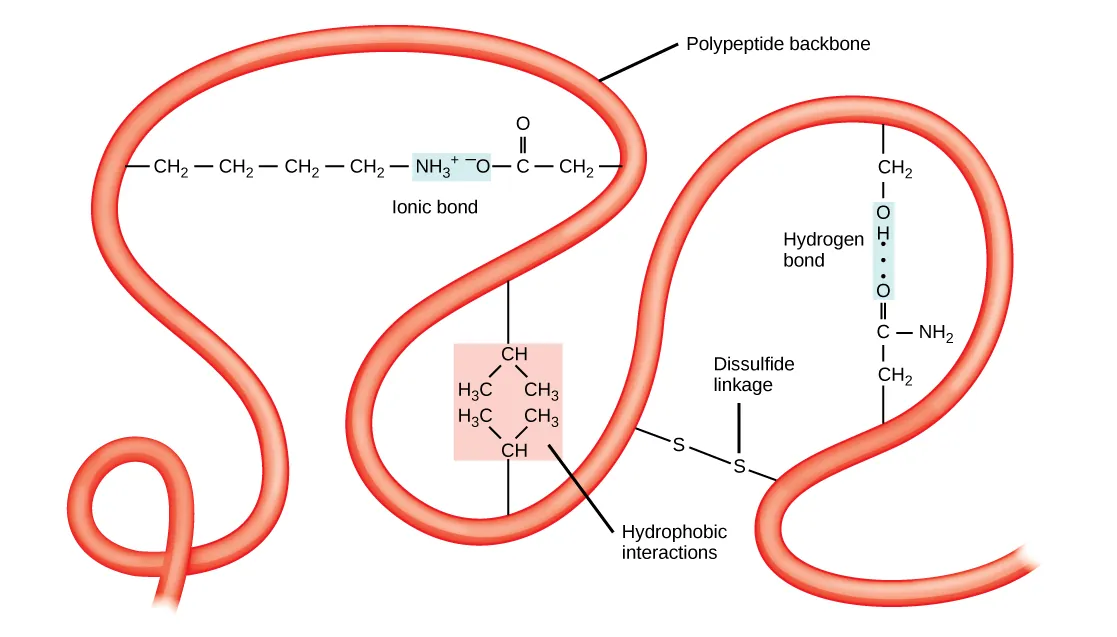
Trong tự nhiên, một số protein được hình thành từ nhiều chuỗi polypeptide, hay còn được gọi là các tiểu đơn vị. Và sự tương tác giữa các tiểu đơn vị này sẽ tạo nên cấu trúc bậc 4. Ví dụ, insulin (một protein hình cầu) được tạo nên từ sự kết hợp của các liên kết hydro và liên kết disulfide khiến nó kết tụ lại thành hình cầu.
Lúc này, nếu như một protein bị “phơi nhiễm” trước sự thay đổi về nhiệt độ, độ pH hoặc tiếp xúc với các hóa chất khác, cấu trúc của protein sẽ bị thay đổi và mất đi hình dạng ban đầu, một quá trình được gọi là biến tính. Một số biến tính thì có thể đảo ngược được nếu các tác nhân kích thích được loại bỏ, cho phép protein tiếp tục thực hiện các chức năng của nó. Nhưng đôi khi một số biến tính lại không thể đảo ngược được, chẳng hạn như chiên trứng – khi protein albumin trong lòng trắng trứng sẽ bị biến tính khi bạn cho nó vào chảo nóng.
Axit nucleic
Cuối cùng, chúng ta hãy cùng nhau phân tích axit nucleic – một “bản thiết kế” hay “nhạc trưởng” của sự sống.
Hai loại axit nucleic chính là axit deoxyribonucleic (DNA) và axit ribonucleic (RNA). DNA là một vật liệu di truyền xuất hiện bên trong tất cả các sinh vật sống. Nó nằm trong nhân tế bào của sinh vật nhân chuẩn và trong các bào quan như lục lạp và ty thể. Ở sinh vật nhân sơ, DNA không được bao bọc bên trong một màng tế bào.
Ở các tế bào nhân chuẩn, DNA tạo thành phức hợp với protein histone để tạo thành chromatin, một chất cấu tạo nên nhiễm sắc thể của tế bào nhân chuẩn. Một nhiễm sắc thể có thể chứa hàng chục nghìn gen với rất nhiều gen trong số này chứa các “chỉ dẫn” để tạo ra các protein. Một số các gen khác thì lại “mã hóa” cho các sản phẩm RNA. DNA có thể kiểm soát tất cả các hoạt động của tế bào bằng cách “bật” hoặc “tắt” các gen nhất định.
Loại axit nucleic còn lại, RNA, chủ yếu tham gia vào quá trình tổng hợp protein. Các phân tử DNA không bao giờ rời khỏi nhân tế bào mà thường sử dụng một chất trung gian để “giao tiếp” với phần còn lại của tế bào. Chất trung gian này là mRNA (message RNA). Các loại RNA khác, chẳng hạn như rRNA, tRNA và microRNA, sẽ tham gia vào quá trình tổng hợp protein và điều hòa hoạt động của nó.
DNA và RNA được cấu tạo từ các monomer mà các nhà khoa học gọi là nucleotide. Sau đó, các nucleotide sẽ kết hợp với nhau để tạo thành polynucleotide, tức là DNA hoặc RNA. Mỗi nucleotide bao gồm ba thành phần: một bazơ nitơ, một đường pentose (năm carbon) và một nhóm phosphate. Bazơ nitơ sẽ được gắn với một phân tử đường, và phân tử đường này sẽ lại được gắn với một hoặc nhiều nhóm phosphate.
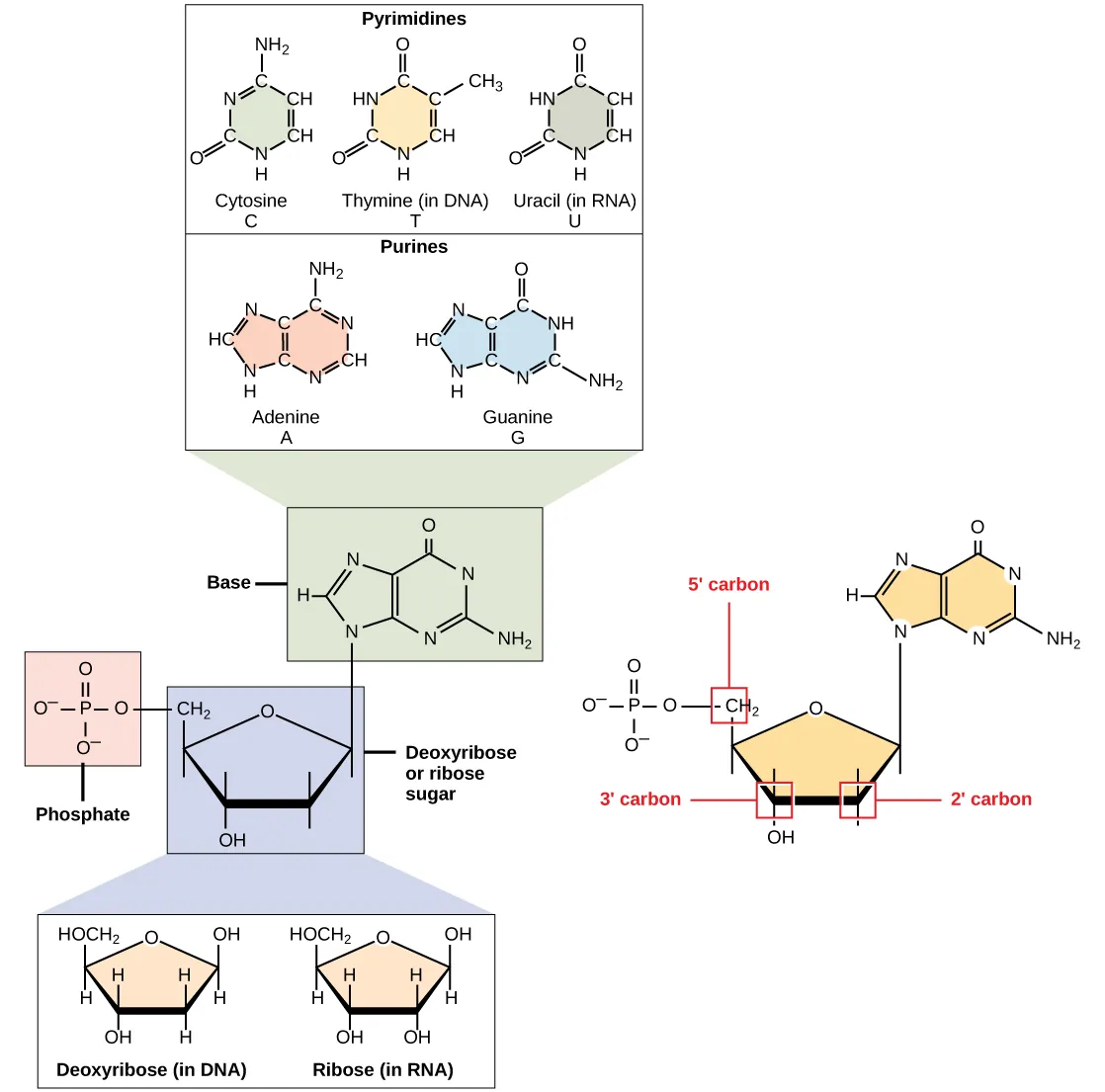
Thành phần đầu tiên, các bazơ nitơ, là một thành phần rất quan trọng của các nucleotide. Sở dĩ chúng được gọi là bazơ vì chúng chứa một nhóm amino có khả năng liên kết với một nguyên tử hydro dư thừa, do đó làm giảm nồng độ ion hydro (H+) trong môi trường xung quanh, làm cho môi trường trở nên kiềm hơn (sự suy giảm nồng độ ion H+ tự do sẽ làm tăng tính bazơ như chúng ta đã đề cập trong bài viết về nước). Có bốn loại bazơ nitơ chính, bao gồm: adenine (A), guanine (G), cytosine (C) và thymine (T).
Thành phần thứ hai chính là đường pentose. Trong DNA, đường này là deoxyribose; còn trong RNA, đường này là ribose. Sự khác biệt giữa hai loại đường này chính là sự hiện diện của nhóm hydroxyl (OH) trên cacbon thứ hai của ribose và hydro (H) trên carbon thứ hai của deoxyribose.
Các nguyên tử cacbon của phân tử đường thường được đánh số là 1′, 2′, 3′, 4′ và 5′. Gốc phosphate thường gắn vào nhóm hydroxyl (OH) của cacbon 5′ trong một phân tử đường và nhóm hydroxyl của carbon 3′ trong phân tử đường thuộc nucleotide tiếp theo, tạo thành liên kết phosphodiester 5′ – 3′. Và một polynucleotide có thể có hàng nghìn các liên kết phosphodiester như thế này.
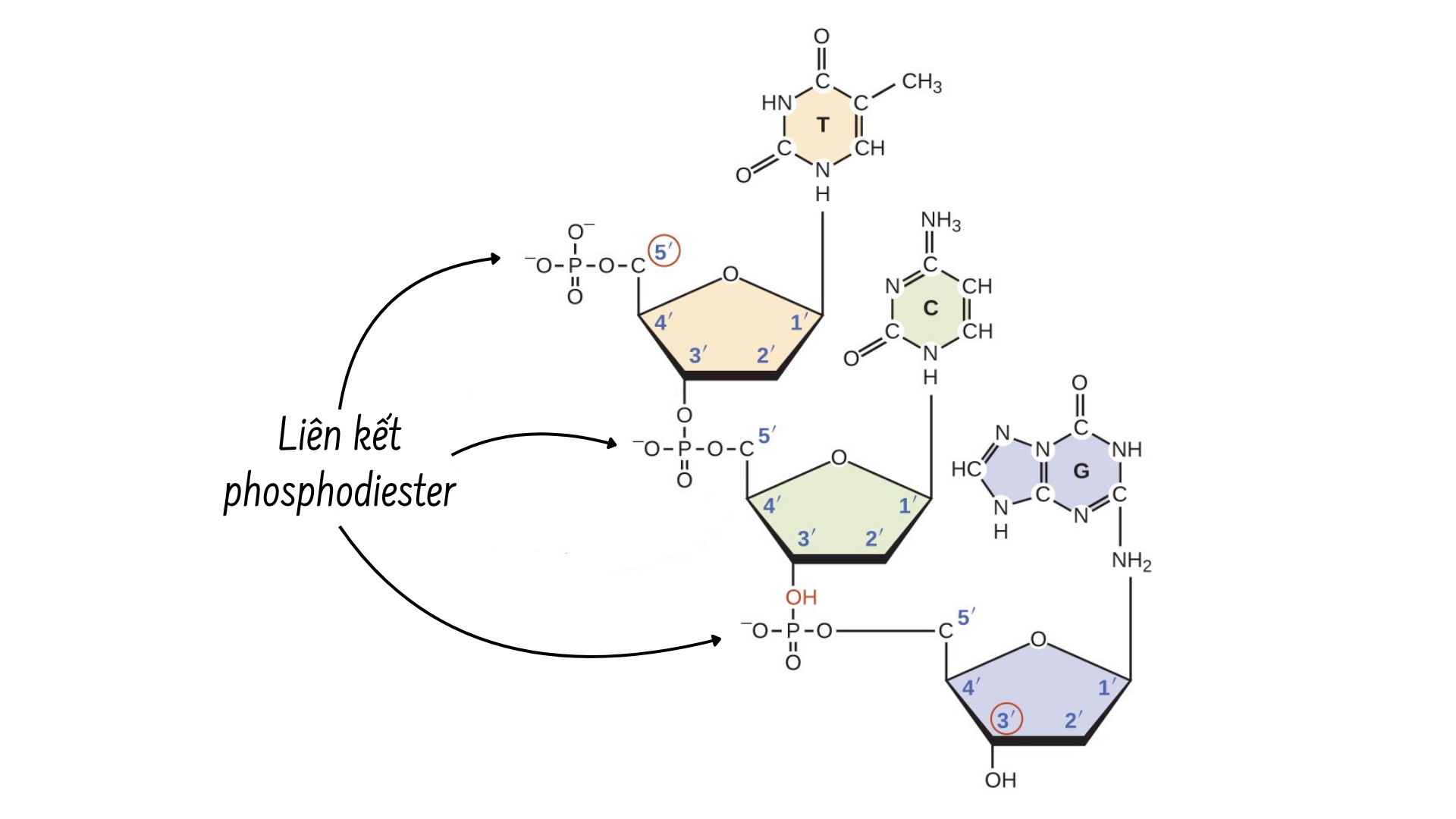
DNA thường có một cấu trúc xoắn kép. Đường và phosphate nằm ở bên ngoài chuỗi xoắn, tạo thành “bộ khung” của DNA. Các bazơ nitơ được liên kết với nhau ở bên trong, sử dụng các liên kết hydro để tạo thành các “bậc thang”. Mỗi cặp bazơ trong chuỗi xoắn kép này cách nhau khoảng 0,34 nm.
Hai sợi của chuỗi xoắn kép này chạy theo hai hướng ngược nhau, nghĩa là một sợi sẽ bắt đầu “chạy” từ đầu carbon 5′ và sợi còn lại sẽ bắt đầu “chạy” từ đầu carbon 3′.
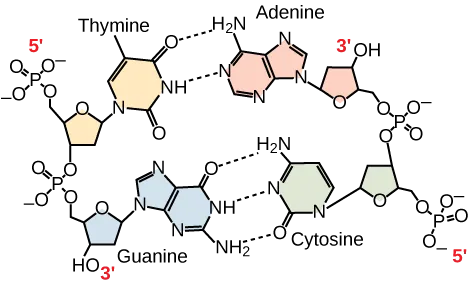
Đối với bazơ nitơ, chỉ có một số ít các cặp bazơ được “liên kết” với nhau. Điều này có nghĩa là A có thể ghép cặp với T; và G có thể ghép cặp với C. Đây được gọi là quy tắc bổ sung bazơ – tức là các chuỗi DNA sẽ bổ sung cho nhau. Ví dụ, nếu như trình tự của một chuỗi là AATTGGCC thì chuỗi bổ sung sẽ có trình tự TTAACCGG.
Axit ribonucleic, hay RNA, chủ yếu tham gia vào quá trình tổng hợp protein dưới sự “chỉ đạo” của DNA. RNA thường là chuỗi đơn và được cấu tạo từ các ribonucleotide kết nối với nhau bằng liên kết phosphodiester. Một ribonucleotide trong chuỗi RNA chứa ribose (đường pentose), một trong bốn bazơ nitơ (A, U, G và C) và nhóm phosphate.
Có bốn loại RNA chính. Loại đầu tiên, mRNA sẽ có nhiệm vụ mang thông tin từ DNA và giúp điều phối tất cả các hoạt động bên trong tế bào. Nếu một tế bào cần tổng hợp một loại protein nhất định, gen mã hóa “sản phẩm” này sẽ được “bật” và mRNA sẽ được tổng hợp trong nhân tế bào. Và trình tự bazơ của RNA này sẽ bổ sung cho trình tự bazơ của DNA mà đang sao chép từ đó. Tuy nhiên, trong RNA, bazơ T bị thiếu và được thay thế bởi bazơ U. Ví dụ, nếu chuỗi DNA có trình tự AATTGCGC thì trình tự của mRNA sẽ là UUAACGCG. Đây được gọi là quá trình phiên mã.
Lúc này, sau khi đã ra khỏi nhân và đi vào trong tế bào chất, mRNA sẽ tương tác với ribosome và các bộ máy tế bào khác. Bây giờ, mRNA sẽ được “đọc” theo từng nhóm – mỗi nhóm sẽ gồm có 3 bazơ nitơ liên tiếp, thường bắt đầu với AUG và được gọi chung là codon. Và mỗi codon sẽ mã hóa cho một axit amin duy nhất. Bằng cách này, mRNA sẽ được “đọc” và protein sẽ được tạo ra. Đây được gọi là quá trình dịch mã.
RNA ribosome (rRNA) là thành phần chính tạo nên ribosome (chiếm khoảng 60% ribosome; 40% còn lại được làm nên bởi protein), liên kết với mRNA và đảm bảo mRNA và ribosome đang đứng ở đúng vị trí. rRNA cũng có hoạt tính enzyme (peptidyl transferase) giúp hình thành liên kết peptide giữa hai axit amin được sắp xếp thẳng hàng.
RNA vận chuyển (tRNA) là các phân tử tương đối nhỏ, dài từ 70–90 nucleotide. Nhiệm vụ của nó là vận chuyển các axit amin đến vị trí tổng hợp protein một cách chính xác.
Cuối cùng, microRNA là các phân tử RNA nhỏ nhất. Nhiệm vụ của chúng là giúp điều hoà quá trình biểu hiện gen bằng cách gắn vào các mRNA, từ đó gây ức chế hoặc phân hủy mRNA.
Đến lúc này, chúng ta đã có trong tay các “mảnh ghép” hóa học quan trọng nhất giúp “nhào nặn” nên sự sống. Và những hiểu biết này chính là chìa khóa giúp chúng ta có thể trả lời cho câu hỏi: Sự sống bắt đầu xuất hiện trên Trái Đất như thế nào?
1. https://en.wikipedia.org/wiki/Life
2. https://en.wikipedia.org/wiki/Virus
3. https://www.ifaw.org/journal/fascinating-animal-adaptations
4. https://www.iaea.org/newscenter/news/what-is-an-atom
5. https://en.wikipedia.org/wiki/Atom
6. https://www.iaea.org/newscenter/news/what-are-isotopes
7. https://pubchem.ncbi.nlm.nih.gov/periodic-table/#view=table
8. https://en.wikipedia.org/wiki/Periodic_table
9. https://winter.group.shef.ac.uk/orbitron/
10. https://www.britannica.com/science/orbital
11. https://en.wikipedia.org/wiki/Chemical_bond
12. https://www.masterorganicchemistry.com/2010/10/06/functional-groups-organic-chemistry/
13. https://en.wikipedia.org/wiki/Hydrocarbon
14. https://www.britannica.com/science/monomer
15. https://en.wikipedia.org/wiki/Carbohydrate
16. https://my.clevelandclinic.org/health/articles/15416-carbohydrates
17. https://medlineplus.gov/carbohydrates.html
18. https://www.ncbi.nlm.nih.gov/books/NBK459280/
19. https://my.clevelandclinic.org/health/body/24425-lipids
20. https://www.ncbi.nlm.nih.gov/books/NBK525952/
21. https://www.britannica.com/science/lipid
22. https://my.clevelandclinic.org/health/body/proteins
23. https://medlineplus.gov/genetics/understanding/howgeneswork/protein/
